| De cara a planificar y entender la clínica
y el tratamiento de micosis fungoide es bueno entender cual es la visión
actual del origen y comportamiento de los linfocitos T neoplásicos en esta
enfermedad. Sabemos que la micosis funogoide es una proliferación clonal
de linfocitos T CD4+, epidermotropos que mantienen varias de las
características de los linfocitos T normales involucrados en las reaccione
inmune cutáneas, hay que entender el papel de los linfocitos T en las
reacciones inmunes cutáneas y su papel como vigilante inmune. |
|
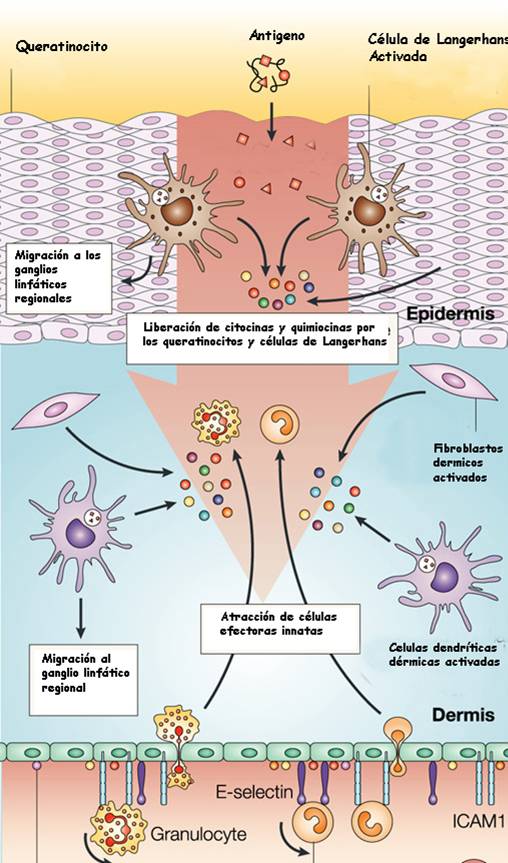
En situaciones normales. Los linfocitos T son
reclutados a la piel tras un daño infeccioso o inmune. Tras el contacto
con un antígeno o un agente infeccioso, se produce una liberación de
citocinas epidérmicas lo cual estimula la respuesta de las células inmunes
residentes como las células dendríticas, mastocitos y macrófagos. Esta
respuesta puede ser mediada por componentes patógenos (bacteriano,
virales) que se reconocen por los receptores de reconocimiento de patrón. El resultado de esta activación es
la producción de diversas células inflamatorias con el reclutamiento y
migración de las células de presentación antigénica hacia los ganglios
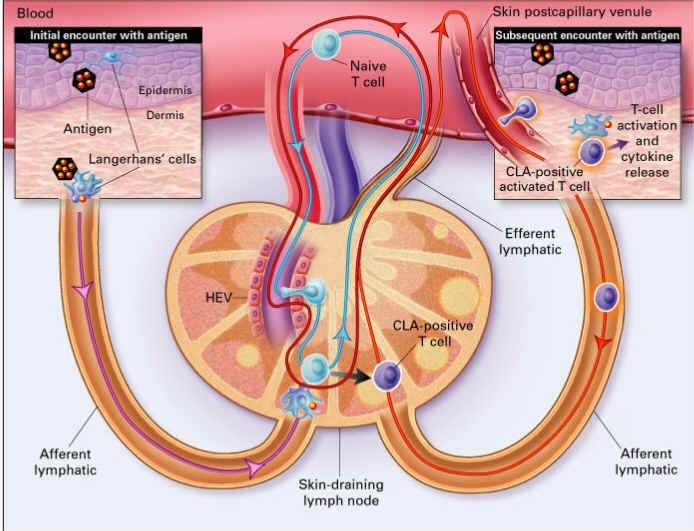
linfáticos de drenaje. Una vez estas células de presentación antigénica
encuentran las células T indiferenciadas en los ganglios linfáticos, se
pone en marcha la respuesta inmune adaptada y se produce una clona de
células de memoria especificas que circulan por el organismos y otras
centrales que actúan como reservorio para la vigilancia inmune.
Estas células de memoria/efectoras expresan el antígeno leucocitario cutáneo (CLA)
y el CCR4 y en situaciones normales representan el 30% de todas las células T de
memoria. Y en situaciones normales no solo acuden a la piel como respuesta a un
estímulo antigénico sino que también habitan la piel como su hábitat normal.
El equilibrio entre las respuestas inmunes de defensa apropiada o inapropiada
con la base para entender la patogénesis y el tratamiento de diversas
enfermedades inflamatorias incluyendo la micosis fungoide.
En este sentido hay que observar la micosis fungoide como una neoplasia de
linfocitos T ue en muchos aspectos funcionan como si estuviesen en condiciones
normales pero que su comportamiento está dominado por su propensión a
localizarse en la piel , ser activados y persistir en un estado activado, llegar
a un estado clonal, acumulándose en la piel ganglios linfáticos y sangre
periférica.
|
|
Este proceso de reconocimiento de antigenos y de respuesta con la formación de
clonas de células con especificidad frente a ese antígeno y con tendencia a la
localización cutánea es la base patogénica de varias enfermedades
cutáneas que comparten datos clínicos e histológicos con la micosis fungoide,
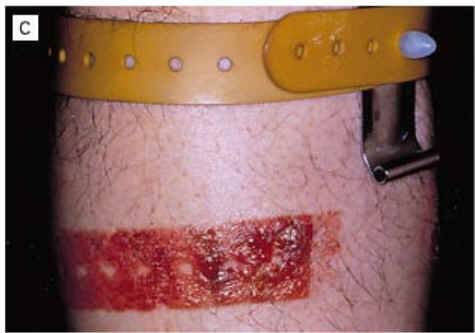
como pueden ser la dermatitis de contacto alérgica, la psoriasis y la dermatitis atopica entre otras. En el caso de la dermatitis de contacto alérgica. Un
paciente que previamente se ha sensibilizado a las gomas con un contacto
posterior sus células dendriticas captan el antígeno y lo presentan a las
células T de memoria circulantes que inician el proceso inflamatorio que
nosotros observamos como una dermatitis de contacto alérgica. En estos pacientes
ha habido una fase aferente en que el paciente se ha sensibilizado y una fase
eferente en el que el paciente sensibilizado responde con el proceso
inflamatorio que se observa clínicamente como eczema. |
|
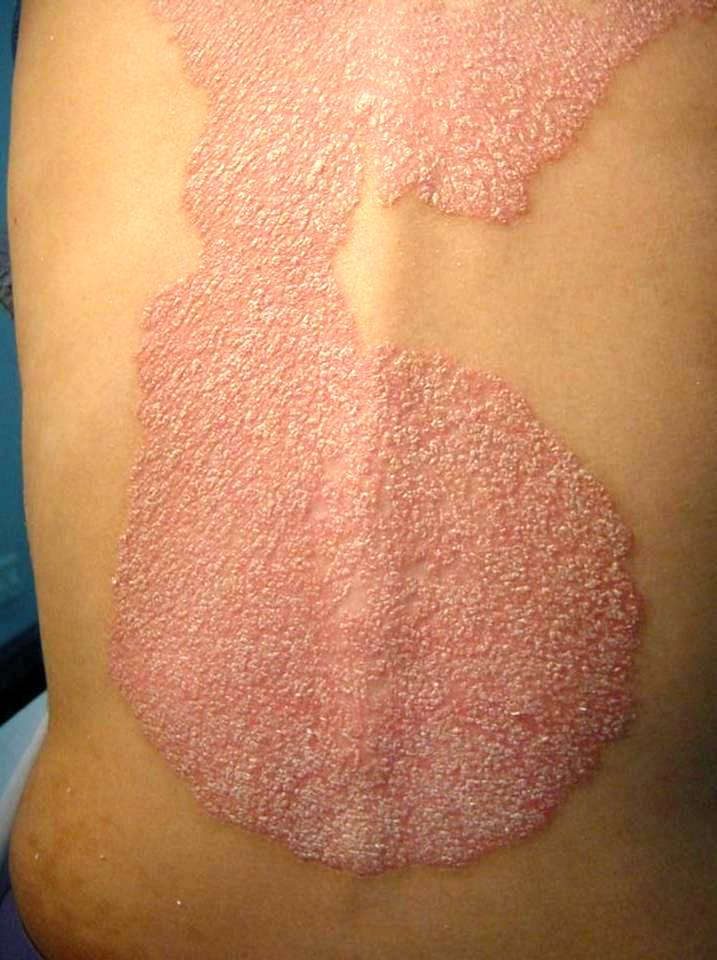
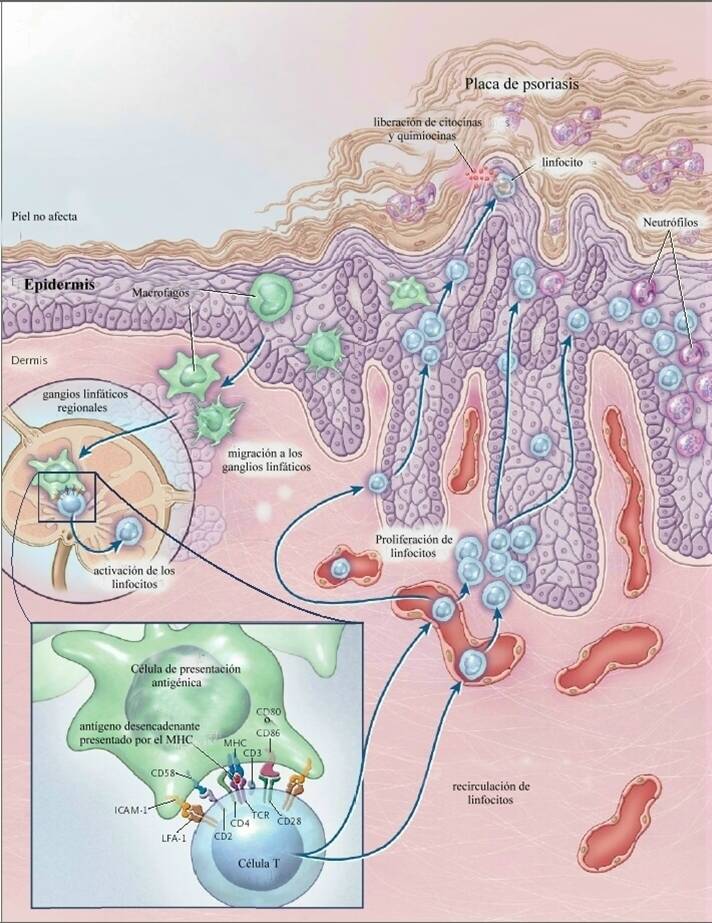
En la psoriasis caracterizada por estas placas eritematosas bien delimitadas de
tamaño variable con una localización característica, que anteriormente se
pensaba que era una enfermedad debida a la proliferación epidérmica y que en la
actualidad sabemos que esta proliferación epidérmica es respuesta a la actividad
de las citocinas liberadas por la infiltración linfocitaria en respuesta a
diversos antígenos.
|
|
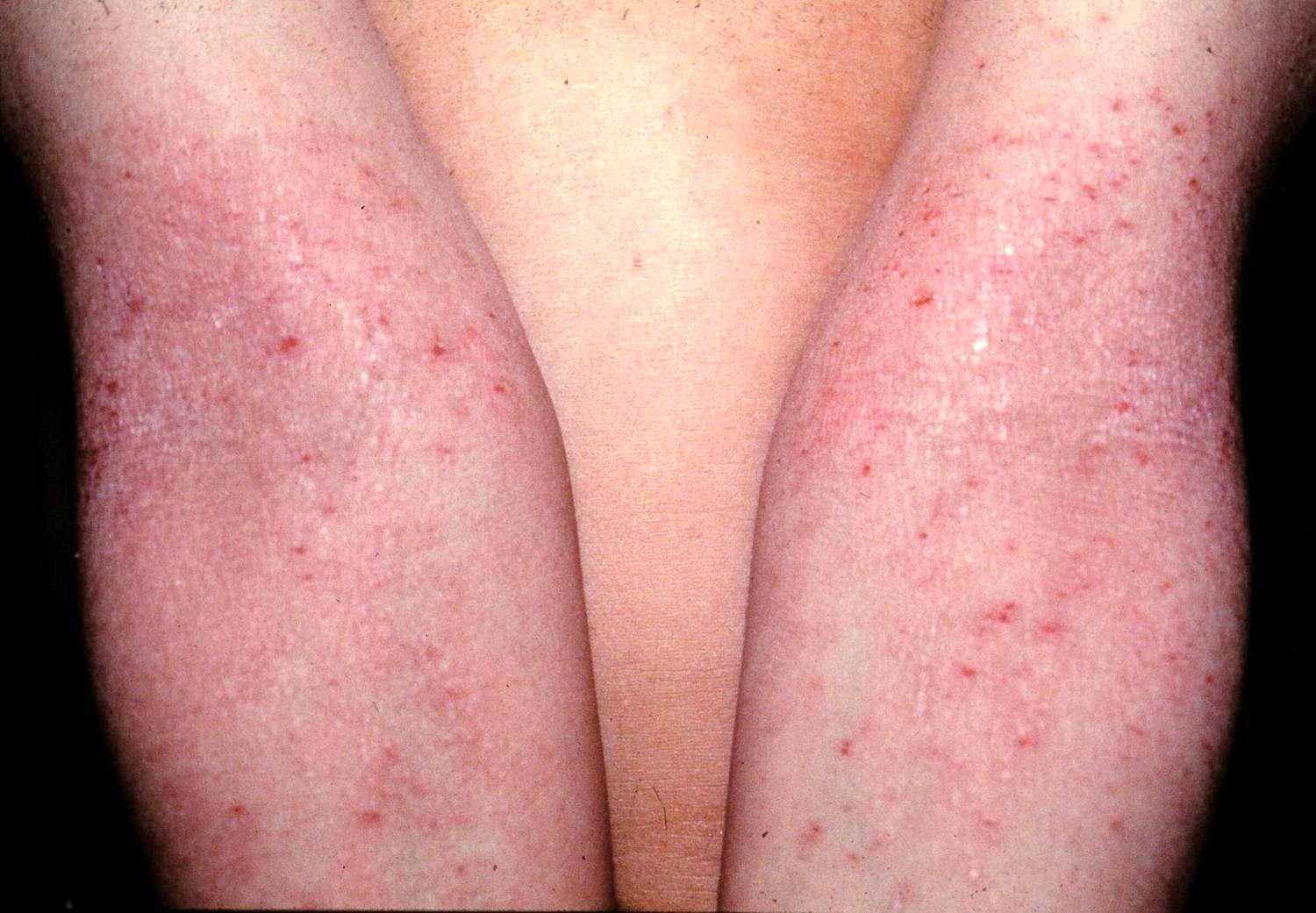
Y también en la dermatitis atopica en la cual ante diversos antigenos se produce
una respuesta inlamatoria mediada por linfocitos T |
|
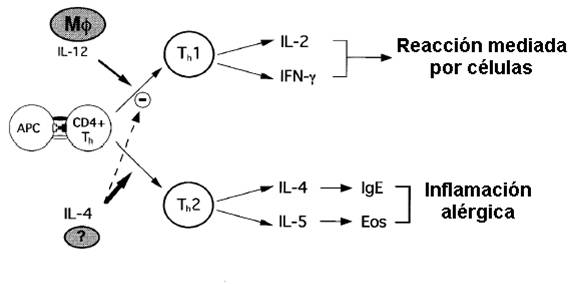
Tras el contacto con la piel, los alergenos son presentados a las células T
indiferenciadas (Th0) en el ganglio linfático por parte de las células de
Langerhans. Como respuesta a la presentación antigénica, las células Th
(Linfocitos T cooperadores) pueden producir dos patrones de citocinas diferentes
que dividen a los linfocitos T en dos subgrupos los Th1 y los Th2.
Las citocinas inflamatorias involucradas en las respuestas alérgicas son
producidas especialmente por el subgrupo de células Th2, mientras que las
citocinas producidas por las células Th1 tienden a antagonizar las respuestas
inflamatorias alérgicas. El predominio de la respuesta de células Th2 viene
determinado por varios factores entre los que se incluyen el aumento de
producción de IL-4, la baja producción de IL-12 por parte de las células de
langerhans y factores producidos por las células epidérmicas. Los Th2 producen
varias citocinas como la interleucina 4 y la IL 13, que son potentes
estimuladores de la producción de IgE y la interleucina 5 que es necesaria para
el crecimiento y diferenciación de eosinófilos. Los linfocitos Th1 son
producidos en presencia de niveles altos de IL-12 y producen interleucina 2,
interferon γ, factor de necrosis tumoral alfa, linfotoxina, y otras citocinas
que promueven las respuestas inmunes contra los patógenos intracelulares y
inhiben la síntesis de IgE por parte de las células B. En las lesiones cutáneas
de dermatitis atópica se encuentra un predominio de linfocitos Th2, lo cual
produciría una producción aumentada de interleucina 4 y de IgE, lo que
caracteriza a las fases agudas de la enfermedad. En la micosis fungoide se
produce una proliferación clonal de linfocitos T CD4+, con especificidad cutánea
que segregan un patrón de citocinas con predominio de clase TH2 semejante a la
dermatitis atopica. |
|
Este comportamiento inmune de los linfocitos T de la micosis fungoide nos ayuda
a explicar que clínicamente las lesiones semejen frecuentemente las lesiones
inflamatorias de estas enfermedades, especialmente del eczema crónico o
dermatitis atpica como esta paciente que estuvo diagnosticad de eczema crónico
durante un largo periodo de tiempo hasta que se pudo establecer el diagnostico
de linfoma cutaneo d ecélulas T . Además el patrón de citocinas en la MF es
semejante a la dermatitis atopica, con un predominio de reacciones TH2,
especialmente en las fasese as su patron de citocinas sea de clase Th2
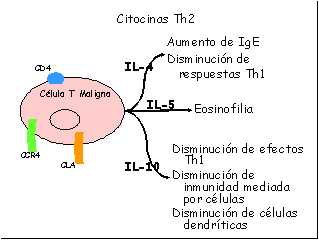
En la micosis fungoide, las células T malignas, CD4+, CLA+, CCR4+, producen
citocinas como la IL-4, IL5, IL-10, lo que da lugar a reacciones tipo Th2 y
subsecuentemente a alteraciones de la inmunidad celular. creando una situación de inmunosupresión que se hace evidente
clínicamente por la mayor propensión a las infecciones cutáneas o por la mala
progresión de la enfermedad cuando se administra a estos enfermos
inmunosupresores sistémicos como la ciclosporina.
|
|
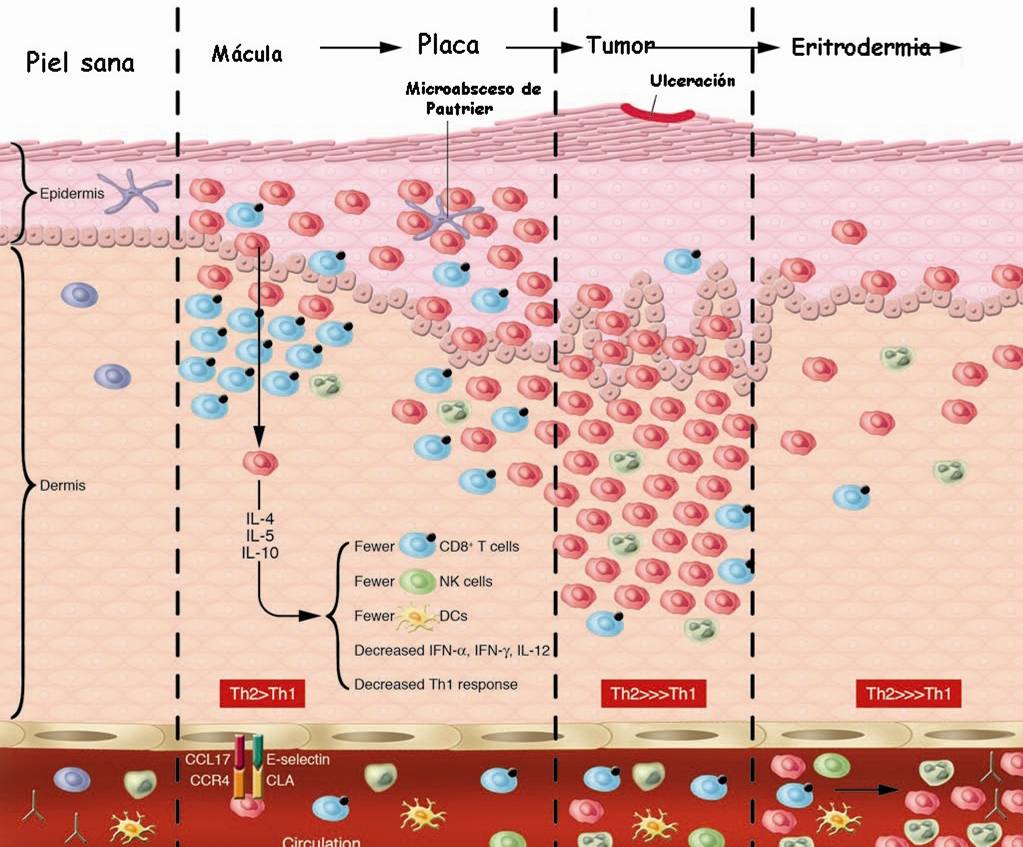
La progresión del infiltrado en la micosis fungoide también varia en el curso de
la enfermedad, al igual que en la dermatitis atopica. Así en las fases iniciales
de la enfermedad cuando estamos en estadios maculares o en placa existe una
proliferación clonal de estas células con marcado epidermotropismo especialmente
alrededor de las células de Langerhans. Es interesante observar que en estas
fases de la enfermedad en el infiltrado existe una marcada presencia de
linfocitos T CD8 + que representan la respuesta inmune al tumor. A medida que la
enfermedad progresa hacia estadios tumorales invade dermis y tejido graso
subcutáneo y se reduce significativamente el infiltrado de células T CD8+. En
las fases eritrodermicas de la enfermedad con células neoplásicas circulantes
productoras de citocinas Th2 que afectan el funcionamiento de las células CD8 y
NK y por tanto la respuesta inmune antitumor.
|

|
Asi pues cuando nos enfrentamos a un paciente con el diagnóstico clínico de
micosis fungoide, confirmado histológicamente de esta enfermedad. Sabemos que en
ese paciente existe una proliferación clonal de linfocitos T CD4+, con
especificidad cutánea con un patrón de citocinas características, que sufren una
estimulación crónica por parte de las células de Langerhans que hace que se
acumulen en los microabscesos de Pautrier y que en el curso de la enfermedad
existe una reducción de células citotoxicas y una inmunosupresion. Estos datos
nos permiten establecer los objetivos en el tratamiento de la MF que seran por
un lado reducir la población clonal de linfocitos T malignos, reducir la
estimulación crónica por parte de las células de Langerhans, revertir la
desvicación Th2 hacia una Th1 y estimular la población de linfocitos T CD8+. |