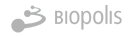El reforç de la vigilància genòmica del SARS-CoV-2 ha sigut recolzat per l'Organització Mundial de la Salut (OMS) per a incrementar la capacitat de detectar noves amenaces i aconseguir accions de salut pública de qualitat, oportunes i adequades.
La detecció de virus patògens per a humans en aigües residuals és una eina molt útil i coneguda per a la vigilància epidemiològica.
Els objectius d'aquesta plataforma seran la identificació de mutacions associades a canvis epidemiològics/clínics de SARS-CoV-2 amb especial atenció a la fallada vacunal.
Som part d'un esforç conjunt centrat en comprendre millor els efectes de les mutacions en el SARS-CoV-2 en temps real. Aquesta beca busca establir una plataforma per a bregar amb amenaces actuals i futures.
Som part d'un esforç conjunt centrat en establir una plataforma per al garbellat d'antivirals contra amenaces víriques actuals i futures. El treball combina grups que s'encarreguen del sencer procés de descobriment i desenvolupament de fàrmacs.
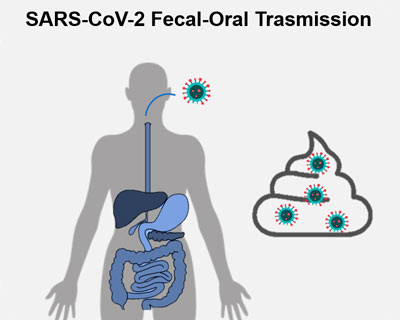
El SARS-CoV-2 és principalment un virus respiratori, encara que s'ha demostrat que pot replicar en la mucosa intestinal, i ser excretat via fecal. Dades moleculars han demostrat la presència de material genètic del virus en femta, mentre que els estudis de detecció de partícules virals infectives són encara incipients i, basats en un número molt xicotet de pacients.
El grup de la Dra. Mar Siles Lucas en la IRNASA maneja models in vitro i in vivo d'interaccions paràsit-hoste amb fasciola hepàtica, que podrien utilitzar-se per a avaluar el potencial del paràsit i les seues molècules per a modular les rutes d'entrada i les rutes d'inflamació rellevants en COVID-19. D'una banda, aquest paràsit ha demostrat la seua influència en l'expressió de les molècules relacionades amb l'endocitosi (per exemple, clatrines) en les cèl·lules epitelials de ratolins in vitro, rutes que poden ser pertinents per a l'entrada del SARS-Cov-2 en les cèl·lules humanes. A més, F. hepàtica dóna lloc a una resposta Th2 modificada sense el component inflamatori en el seu hoste in vivo, i aquesta modulació pot donar lloc a una resposta inflamatòria controlada a la COVID-19.
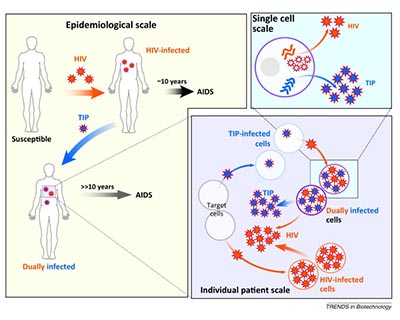
Les partícules d'interferència defectuoses (DIP) són formes degenerades de genomes virals que no es reprodueixen però que continuen sent infeccioses per la complementació amb el virus de tipus salvatge (TW). Les DIP exerceixen un paper important en la modulació del resultat de la infecció i les respostes immunitàries, i poden seleccionar-se artificialment per a reforçar la seua activitat d'interferència i suprimir la replicació del virus complet (partícules d'interferència terapèutica, o TIP per les seues sigles en anglés). Proposem produir DIPs durant la replicació del SARS-CoV-2 en cultiu cel·lular, purificar-les, provar els seus efectes antivirals i caracteritzar-les molecularment. El resultat del projecte serà un conjunt específic de TIPs per al SARS-CoV-2 que podria utilitzar-se immediatament per a tractar el COVID19.
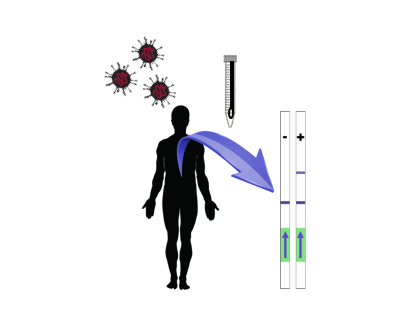
Les tècniques tradicionals de diagnòstic d'infeccions virals en la clínica es basen en procediments de (RT-)PCR, que porten molt temps i requereixen equip i recursos humans molt precisos, la qual cosa impedeix una intervenció ràpida i massiva. En aquest article, dissenyarem una nova classe de biosistemes autònoms destinats a diagnosticar la presència del SARS-CoV-2. Aquests biosistemes consisteixen en tres passos de reacció després de la recollida de la mostra sense necessitat d'un equip sofisticat: i) amplificació isotèrmica de l'ARN viral, ii) detecció d'àcids nucleics basada en el CRISPR (que funciona com una reacció de seqüenciació sobre la marxa), i iii) revelació de resultats mitjançant un assaig inmunocromatogràfic.
Encara que el SARS-CoV-2 i uns altres coronavirus es transmeten fonamentalment de manera directa entre individus durant les fases epidèmiques, la permanència del virus en l'ambient té el potencial d'originar nous brots malgrat els esforços de mitigació desplegats. El SARS-CoV-1 es va detectar en aigües residuals d'hospitals a la Xina i es va demostrar que les partícules virals podien romandre infectives el suficient temps com per a constituir un risc.
En aquesta col·laboració s'aplicarà un enfocament multidisciplinari per a identificar els inhibidors de la unió i l'entrada del receptor del SARS-CoV-2. Combinant els coneixements de la química mèdica, la biologia química computacional, la biologia estructural i la virologia, s'empraran tres enfocaments paral·lels: 1) Assaig immediat de les biblioteques de compostos (>1.400) mitjançant un assaig cel·lular d'alt rendiment per a la unió i entrada del receptor del SARS-CoV-2. 2) Examen i disseny, síntesi i avaluació computacionals (3). Desenvolupament d'inhibidors basats en proteïnes derivats del receptor ACE2. L'avaluació final dels èxits quant a eficàcia i resistència als medicaments es farà amb el SARS-CoV-2.
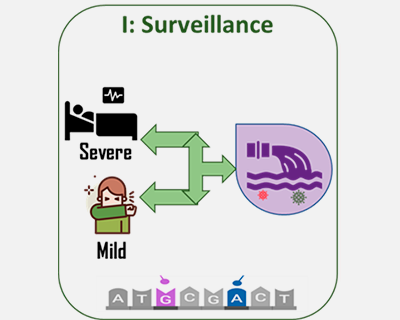
El projecte científic liderat per investigadors del Consell Superior d'Investigacions Científiques (CSIC) en col·laboració amb 40 hospitals de tota Espanya estudiarà els genomes comparats del nou coronavirus de pacients amb malaltia Covid19 per a entendre i predir l'evolució i epidemiologia del virus.
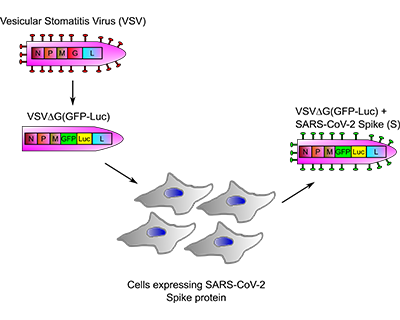
El projecte proposa una nova estratègia per al garbellat de fàrmacs i anticossos contra el coronavirus SARS-CoV-2. Es tracta d'una tecnologia innovadora per a garbellat de fàrmacs que utilitza un sistema econòmic, ràpid, segur i eficient per a avaluar tot tipus de compostos antivirals i anticossos que bloquegen l'entrada del virus SARS-CoV-2 en les cèl·lules humanes. La utilització de virus recombinants ha sigut emprada amb èxit en el garbellat de fàrmacs enfront de diferents virus d'importància mèdica, així com en el garbellat serològic. Els avantatges de la proposta estan ben fonamentades, destacant que aquesta tecnologia pot ser aplicable en el futur a altres virus que constituïsquen un problema de salut pública emergent.


 EvolCovid
EvolCovid
 PTI+: Transmissió i contenció
PTI+: Transmissió i contenció
 Vigilància genòmica
Vigilància genòmica
 Mutaciones
Mutaciones
 Antiviral platform
Antiviral platform
 FecOrSARS
FecOrSARS
 COVID-19: acció antiinfecciosa i antinflamatoria de les molècules del paràsit immunomodulador en un format sintètic d'ús segur
COVID-19: acció antiinfecciosa i antinflamatoria de les molècules del paràsit immunomodulador en un format sintètic d'ús segur
 CoV2TIP
CoV2TIP
 COV-CRISPIS
COV-CRISPIS
 EnvironmentalCOVID
EnvironmentalCOVID
 BlockAce
BlockAce
 SeqCOVID
SeqCOVID
 ANTICOR
ANTICOR