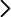Grupo de investigacióm: TheSiMBioSys
La resistencia a los antibióticos y la ingeniería de tejidos/medicina regenerativa han sido reconocidas como dos de los grandes retos de investigación de la Biotecnología. Aunque aparentemente inconexos, argumentamos que proporcionar respuestas cuantitativas a estas cuestiones requiere un enfoque común desde el punto de vista de la mecanobiología. Por un lado, la lectura fenotípica característica de la resistencia a los antibióticos (y más en general de la respuesta al estrés en las bacterias) es la filamentación. Esta última se ha vinculado a las estrategias de supervivencia y a la virulencia. Por consiguiente, la comprensión de los procesos que impulsan ese rasgo fenotípico característico puede ser útil para la elaboración de soluciones para hacer frente a este problema y a sus consecuencias (por ejemplo, la formación de biopelículas). En este contexto, se ha ignorado en gran medida el papel que desempeñan las claves biomecánicas durante la filamentación celular. Por otra parte, la medicina regenerativa depende de soluciones del campo de la ingeniería de tejidos y órganos. Esta última es un problema multifactorial que requiere, entre otras cosas, una comprensión profunda de los mecanismos que conforman los agregados celulares. La conformación de un tejido a su vez implica el conocimiento de cómo la dinámica celular impulsa la remodelación colectiva. A ese respecto, los procesos de intercalación celular (ya sea en el tiempo o en el espacio) son fundamentales para comprender la plasticidad de los tejidos. Sin embargo, hasta la fecha, ningún modelo ha explicado de manera convincente cómo los patrones de polaridad estacionarios pueden traducirse en una dinámica de intercalación plana sostenida (transiciones T1 en el tiempo) y, en el contexto de nuestro descubrimiento de los escutoides (transiciones T1 en el espacio), existe una falta de comprensión cuantitativa sobre cómo se regulan las fuerzas y sobre los efectores moleculares subyacentes. Los objetivos específicos de este proyecto son: Objetivo 1: Comprender el papel que desempeñan las retroalimentaciones de mecanoseñalización durante la filamentación de E. coli; Objetivo 2: Comprender el acoplamiento entre el patrón/señalización de los tejidos en los eventos de intercalación celular (en el espacio y el tiempo). Las cuestiones abiertas específicas que abordaremos son: a) la existencia de propiedades mecanosensibles de la maquinaria de división/crecimiento en E. coli para regular su filamentación y diversidad fenotípica, b) los mecanismos que traducen las propiedades de los patrones en la elongación del tejido durante el crecimiento de las yemas de las extremidades, y c) la metodología necesaria para caracterizar las fuerzas y contribuciones energéticas en un contexto tisular tridimensional (3D), y el consiguiente vínculo con los efectores subyacentes y la elaboración de esquemas de simulación tisular realistas.
Javier Buceta
Ministerio de Ciencia e Innovacion