
NÚMERO 3 - 1998 - ARTÍCULO 17

NÚMERO 3 - 1998 - ARTÍCULO 17
![]()
ANÁLISIS DE UNA ALEACIÓN DE GALIO MEDIANTE MICROSCOPÍA ELECTRÓNICA DE BARRIDO Y MAPING EN COLOR DE CADA UNO DE SUS ELEMENTOS.
José Luis Baños Martín*. Vicente Vera Gonzalez**. Juan José Hidalgo Arroquia **. Gabriel García García ***.
* Profesor Titular Interino.
** Profesor Asociado.
*** Colaborador.
Departamento Estomatología II. Odontología Conservadora. Materiales Odontológicos. Universidad Complutense de Madrid.
RESUMEN
Presentamos en este trabajo un método para realizar estudios sobre composiciones de aleaciones mediante microscopía electrónica de barrido con sonda incorporada. Las microfotografías realizadas, al mismo tiempo que son representaciones gráficas de la distribución de los elementos, lo son también de los gradientes de sus concentraciones en la aleación, representados por distintos colores. Hacemos un estudio sobre la distribución de los elementos en una aleación de galio.
PALABRAS CLAVE
Galio. Análisis. Maping. Microscopía electrónica de barrido.
SUMMARY
We present a method to study alloys with scanning electron microscopy with an attached probe. Microphotographs show the distribution of elements and their different concentrations. We present an study of the distribution of elements in a gallium alloy.
KEY WORDS
Gallium. Analysis. Maping. Scanning electron microscopy.
INTRODUCCIÓN
Los resultados de los estudios metalográficos que se hacen sobre las composiciones de aleaciones metálicas en el campo odontológico, se suelen presentar con texto, valores numéricos y fotografías en blanco y negro sobre las cuales se colocan flechas indicadoras acompañadas de letras o números y cuya explicación se da o bien a píe de fotografía o bien en el texto. Mediante este procedimiento somos guiados por la subjetividad del investigador, avalada por sus conocimientos de la materia en cuestión. Tratamos, mediante el procedimiento que aquí presentamos, de permitir al lector interesado de sacar sus propias deducciones además de las del investigador.
MATERIAL Y MÉTODO
Como material de estudio hemos elegido una aleación de galio, poco utilizada a nivel general, cuya particularidad reside en no contener mercurio y que al carecer del efecto tóxico de este, trata de suplir a la amalgama. No entramos a debatir este punto.
Hemos preparado una probeta de aleación de galio con trituración de 10 s de una cápsula comercial de la casa Tokuriki Honten Co. El polvo de la aleación contiene 50% de plata, 26% estaño, 15% cobre y 9% paladio en partículas esféricas de 21 micrómetros de diámetro medio, el líquido está compuesto por 65% galio, 16% estaño y 19% indio. La composición final de la aleación contiene un 30,3 % de plata, 25,61 % de galio, 21,06 % de estaño, 9,09 % de cobre, 7,88 % de indio y 6,06 % de paladio.
Hemos pulido su superficie al cabo de 24 horas y estudiado su superficie, previamente tratada con ácido adecuado, con microscopio electrónico de barrido de la casa J.E.O.L. super probe JXA-8600 y analizado su composición mediante sonda Lynk, de todos y cada uno de sus elementos, realizando microfotografías de su distribución y concentraciones reflejadas en tonos grises cuyas intensidades son transformadas, con un programa informático adecuado, en colores que nos indican la concentración del elemento estudiado en cada caso, siendo esta máxima para el color blanco, decreciendo con el rojo, amarillo, azul y negro, indicando este último ausencia del elemento estudiado.
RESULTADOS
Hemos obtenido seis microfotografías correspondientes a cada uno de los elementos que componen la masa final, donde podemos comprobar tanto su concentración como su distribución de cuyo estudio podremos sacar las conclusiones oportunas en función de la variable a estudiar.
En la primera, correspondiente al paladio observamos que su distribución se limita a las partículas de la aleación del polvo sin salir a los espacios interpartículas, siendo su concentración alta y uniforme.
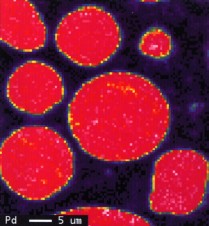
Figura 1. Paladio: distribución y concentración.
En la segunda, correspondiente a la plata, se ve que su distribución corresponde a las partículas, aunque con un menor diámetro que en el caso del paladio, ocupando también parte del espacio interpartículas, siendo su concentración alta en ambas distribuciones.

Figura 2. Plata: distribución y concentración.
En la tercera, correspondiente al cobre, observamos que la distribución corresponde al diámetro de las partículas originales aunque con un halo de menor concentración, encontrándose también de forma irregular en el espacio interpartículas con una alta concentración.
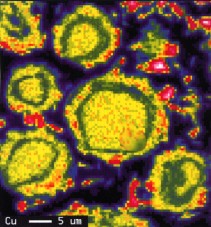
Figura 3. Cobre: distribución y concentración.
En la cuarta, correspondiente al estaño, observamos que ocupa un diámetro menor que en las partículas originales y con baja concentración, en cambio se encuentra en el espacio interpartículas con una alta concentración, pues forma también parte del líquido.
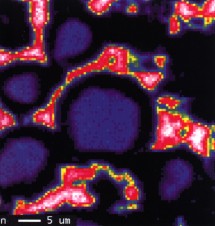
Figura 4. Estaño: distribución y concentración.
En la quinta, correspondiente al galio, vemos que su distribución es alrededor de las partículas entrando en la parte periférica de ellas con una alta concentración, encontrándose también en la zona interpartículas aunque con una muy baja concentración.
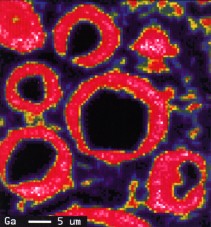
Figura 5. Galio: distribución y concentración.
En la sexta, correspondiente al indio, siendo este un componente del líquido, se encuentra solo en el espacio interpartículas con una alta concentración.
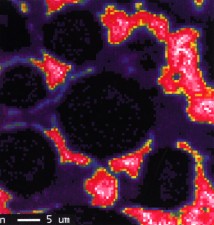
Figura 6. Indio: distribución y concentración.
DISCUSIÓN Y CONCLUSIONES
Consideramos que este puede ser un procedimiento de estudio en cierto sentido de carácter interactivo, donde el lector con los datos aportados puede sacar sus propias deducciones, conclusiones u opiniones.
Una forma de afrontar la cuestión seria la de ver qué elementos ocupan el mismo espacio, así como sus concentraciones relativas lo cual nos podría indicar el grado de solubilidad de unos con otros y la posibilidad de formar compuestos intermetálicos.
A modo de ejemplo podríamos ver que el paladio no reacciona con ningún otro elemento, de ello se podría deducir el porqué de las nuevas aleaciones a base de galio no lo incorporan en su composición.
Otra cuestión es ver el grado de disolución que produce el galio sobre los elementos de las partículas y podemos observar como disuelve a la plata en la periferia de las partículas yendo esta a reaccionar con el indio en el espacio interpartículas.
El presente estudio podría servir de base, en posteriores trabajos, para comprobar distintas propiedades de esta aleación en función del tiempo de trituración y ver los cambios que se producirían en la distribución y combinación de los elementos.
BIBLIOGRAFÍA