1.Younger
IR. Azathioprine in dermatology JAAD 1991 25:281-6
2.Dutz
JP, Ho VC. Immunosuppressive agents in dermatology. Derm clinics 1998 16:235
3.Lear
JT. English JSC, Jons P. Smith AG. Retrospective review of the use of azathioprine
in severe atopic dermatitis. JAAD 35 (4):642-4, 1996
4.Buckley
Da, Baldwin P. Rogers S. The use of azathioprine in severe adult eczema.
JEADV 11 (1998) 137-49
5.Snow
JL, Gibson LE. A pharmacogenetic basis for the safe and effective use of
azathioprine and other thiopurine drugs in dermatologic patients. JAAD
1995:32: 114-6.
6.Snow
JL, Gibson LE. The role of genetic variation in thiopurine methyltransferase
activity and the efficacy and/or side effects of azathioprine therapy in
dermatologic patients. Arch Dermatol 1995 Feb;131(2):193-7
7.Scerri
L. Azathioprine in dermatológica practice. An overview with special
emphasis on its use in non-bullous inflammatory dermatosis. Adv Exp Med
Biol 1999, 455:343-8.
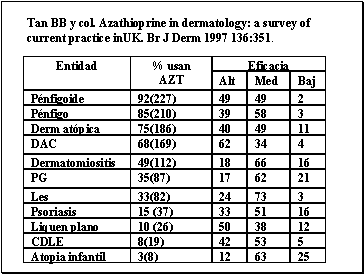
8.Tan
BB y col Azathioprine in dermatology: A survey of current practice in the
UK. Br. J Derma 1997 136:351-5.
Younger
IR. Azathioprine in dermatology JAAD 1991 25:281-6
La azatioprina
es un antipurínico metabolizado a nivel hepático hacia la
6 mercaptopurina y posteriormente a 6-tioinisinico, su metabolito activo.
La azatioprina inhibe la síntesis de DNA y RNA
1-Quimica
y farmacología:
absorción intestinal y rápida conversión a 6-mercaptopurina.
su rango terapéutico más efectivo esta entre 1-2.5 mg/kg./día
existe poco efecto terapéutico por debajo de 1 mg/kg./día
. Existen tres mecanismos de metabolización de la 6 mercaptopurina
|
vías metabólicas
de la azatioprina
|
|

|
1.Xantina
oxidasa: transforma la 6.MP en el metabolito inactivo ácido 6-tiourico
2.Tiopurina
metiltransferasa (TPMT): coniverte la 6-MP en 6-metilmercaptopurina, un
metabolito de actividad no conocida
3.Hipoxantina
fosforibosil transferasa: permite el paso de nucleótidos de 6-tiogunina
(6-TGNS). Estos productos son lo s que se consideran responsables de la
mielotoxicidad de forma idiosincrática.
Existe
una relación inversa entre la actividad de la enzima TPMT y la formación
de 6-TGN. Se puede observar un polimorfismo genético asociada a
dicha actividad. El 0,3% de la población presenta una deficiencia
en su actividad.
|
2-modo de acción:
-
interfiere
con las síntesis de bases purínicas, síntesis de DNA,RNA,
por lo que afecta la división celular
-
inhibe algunas
de las funciones de las células T así como las funciones
de inmunidad celular
-
se inhiben
algunas funciones de los PMN y monocitos
-
se inhiben
numerosas prostaglandinas
3-Interacciones
medicamentosas
-
El alopurinol
inhibe la xantina oxidasa, que es el responsable de la degradación
de la azatioprina por lo que se prolonga su acción, la dosis de
azatioprina debe ser reducida a un cuarto si se utilizan conjuntamente
-
debe ser
utilizada cuidadosamente en enfermos hepáticos
-
si existe
insuficiencia renal debe ser reducida la dosis
-
la acción
de ciertos relajantes musculares de anestesia general se ven alterados
por la azatioprina
-
Supresión
de la médula ósea: generalmente causa leucopenia y ocasionalmente
trombocitopenia o pancitopenia, generalmente ocurren a dosis altas y desaparecen
al reducir la dosis. Nuestra practica es realizar un hemograma completo
cada semana durante el primer mes y entonces una vez al mes
-
:nausea,
vomito y diarrea que mejoran si se toma con alimento o al reducir la dosis
-
hipersensibilidad
:ictericia colostatica, fibrosis portal, necrosis hepatocelular, fiebre
y rash maculopapapular, pneumonitis intersticial, debilidad muscular pancreatitis
y shock
-
puede mimetizar
los efectos de la radioterapia en la piel dando como resultados unos fibroblastos
estrellados en el estroma que pueden ser vistos por el dermatopatologo
-
aumento de
la infección por verruga, HSV, VZ, y sarna noruega
-
Oncogenicidad:
los tipos de tumores que ocurren en pacientes con trasplante renal inmunosuprimidos
con corticoides y azatioprina son:
§Linfoma
12%
§Cáncer
cervical 6%
§kaposi
3%
§cáncer
vulvar 3%
5-Uso
clínico en dermatología:
indicaciones bien establecidas
§Penfigo:
La terapia efectiva más segura parece ser que es la administración
de azatioprina inicialmente a dosis de 2-3 mg/kg./día mas prednisolona
a dosis de 80-200 mg./día, cuando el paciente mejora la dosis de
ambas medicaciones puede ser reducida y tras dos meses de remisión
clínica los esteroides generalmente pueden ser parados
§Penfigoide:
En casos resistentes la azatioprina puede ser una buena medicación
de ayuda
§Eczema
§LE
§DMS/PMS
6-Posologia
La dosis inicial suele estar entre 1 y 2 mg/kg/día, que se puede
reducir en dos dosis para reducir los efectos secundarios digestivos. Si
en 6-8 semanas no hay mejoria la dosis se va incrementando en 0,5 mg/kg/día
cada 4 semanas. La dosis máxima es de 3 mg/kg/día. Una vez
la enfermedad esta estabilizada se irá reduciendo la dosis en 0,5
mg/kg/día cada 2-4 semanas hasta alcanzar la dosis mínima
de mantenimiento.
7-Monitorización
Debe realizarse controles hematológicos y bioquímicos
antes de iniciar el tratamiento y con frecuencia. Las máximas alteraciones
hematológicas suelen presentarse entre el 7º y el 14º
día. El hallazago de una leucopenia de menos de 4000/mm3 o una plaquetopenia
de menos de 150000 obligará a reducir la dosis . Por debajo de 2500
leucos o de 100000 plaquetas debe ser suspendida temporalmente. La determinación
de la actividad de la enzima tiopurina metiltransferasa, evitaría
el riesgo presente en el 0,3% de la población. Esta determinación
se realiza a nivel eritrocitario y ofrece una estimación muy aproximada
de la actividad de la enzima a nivel hepático
Dutz
JP, Ho VC. Immunosuppressive agents in dermatology. Derm
clinics 1998 16:235
Azatioprina
La
azatioprina ha estado disponible durante más de 30 años y
es una de las medicaciones inmuno-moduladoras más utilizadas en
dermatología. Es un análogo sintético de las purinas
que se forma por medio de la unión de un anillo inmidazol a la 6-mercaptopurina
(6-MP) y actúa como una pro-droga ya que es convertida rápidamente
a 6-mercaptopurina por medio de un ataque no-enzimático de los componentes
sulfidrilicos presentes en los eritrocitos y componentes tisulares.
Farmacología
La
azatioprina se absorbe rápidamente tras su administración
oral. Tiene una vida media plasmática de solo 3 horas debido a su
rápida conversión a 6-MP. Sin embargo los metabolitos activos
tiene una vida media larga, permitiendo una sola toma al día. La
6 MP se metaboliza por 3 vías la
1.tiopurina
metiltransferasa (TPMT) cataliza laS-metilizaciónproduciendo
la 6-metil mercaptopurina, que es un componente inactivo
2.Xantina
oxidasaque cataliza la oxidación
para producir el ácido 6-tiourico que es inactivo
3.Hipoxantina-guanina
fosforibosil transferasa (HGPRT) que cataliza la conversión de la
6-MP a los metabolitos activos de la 6 tioguanina
Los
niveles eritrocitarios de nucleótidos de 6-tioguanina se correlacionan
con el recuento absoluto de neutrófilos y se pueden requerir mucho
tiempo para adquirir niveles estables. En la actualidad es bien conocido
que existe un polimorfismo genético que controla la actividad de
la TPMT, el 88,6% de la población es homocigota para un alelo de
gran actividad y el 0,3% es homocigota para un alelo de baja intensidad
de la TPMT. En los pacientes con trasplante renal los niveles bajos de
actividad de la TPMT se correlacionan con una mayor incidencia de leucopenia
debida a la azatioprina y los que tienen niveles más altos tienen
una menor inmunosupresión. Los pacientes con niveles intermedios
tienden a presentar neutropenias de inicio tardío.
Se
ha sugerido que la determinación preterapéutica de la actividad
eritrocitaria de la TPMTpodría
detectar los pacientes(1/300) con
riesgo de una neutropenia de inicio temprano. Esto puede determinarse mediante
test de radioenzima o por cromatografía líquida. Recientemente
el aislamiento y caracterización de mutaciones de alelos causando
un déficit de TPMT ha permitido la identificación de más
del 80% de todos las mutaciones de TPMT y ha permitido el diagnóstico
de déficit de TPMTy el estado
heterocigoto basado en el genotipo. Si la medicación se utiliza
sin la medición preterapéutica de TPMT se recomienda aconsejar
a los pacientes acerca de los riesgos asociados yla
poca idoniedad de los hemogramas para prevenir la toxicidad temprana. Existen
otros factores queafectana
la actividad de la TPMT como son la sulfazalazina y su metabolito 5-aminosalicilico
que inhiben la actividad mientras que la 6-mercaptopurina y los diuréticos
pueden inducir su actividad. Todos los pacientes requieren una terapeutica
personalizada y guiada por el recuento leucocitario y plaquetario.
Los
metabolitos de la 6-tioguanina evitan la intercoversion de las bases purínicas
y inhiben la síntesis de novo de bases purínicas de una forma
específica en la fase S. Este efecto antiproliferativo puede no
ser el único responsable de su acción inmunosupresora ya
que se han demostrado efectos en la función de las células
NK (natural killer), actividad citocínica de las células
T, producción de prostaglandinas y actividad neutrofílica.
No se han demostrado cambios significativos en los niveles de interleucinas.
Efectos secundarios
de la azatioprina
|
Hematológicos
|
Mielosupresión
manifestada como leucopenia, trombocitopenia o pancitopenia. La toxicidad
inicial es de inicio rápido y puede ser prevenida por la medición
preterapéutica de la actividad de la TPMT. La toxicidad tardía
es de inicio lento y puede requerir años para su instauración.
Se observo leucopenia de un 10% (3/29) pacientes con pénfigo vulgar
tratados con una dosis media de 2 mg/kg durante 4-12 años. En unaencuesta
realizada entre dermatólogos de UK, un 45% habían observado
mielosupresión significativa
|
|
|
El
desarrollo de nausea y vómitos es el efecto secundario más
frecuente. Un 8% de pacientes con penfigoide ampolloso tratados con azatioprina
y prednisona mostraron hepatotoxicidad
|
Infecciones
oportunísticas
|
Tiene
una mayor tendencia a desarrollar infecciones incluso en ausencia de leucopenia.
Tienen con mayor frecuencia HSV, VZV y infecciones por papilomavirus
|
|
|
La
AZT se ha asociado con un aumento en la incidencia de neoplasias en los
pacientes trasplantados, incluyendolinfomas,
sarcoma de kaposi, carcinoma renal, de cerviz, vulvar y carcinomas cutáneos.
Sin embargo el estudio comparativo con la CSA sugiere que la mayor incidencia
de neoplasias es comparable y se debería más a la inmunosupresión
que a la medicación utilizada.
|
Reacciones
de hipersensibilidad
|
Esta
es una reacción rara(solo
hay 30 casos descritos) que se inicia entre 3 horas y 42 días tras
tomar la medicación (media de 14 días). Las manifestaciones
incluyen hipotension, shock, erupción cutánea maculopapular,
urticaria y/o vasculítica, fiebre, hepatotoxicidad aguda , pacreatitis,
rabdomiolisus y insuficiencia renal aguda.
|
|
|
Junto
con el isotretinoino se ha descrito el ensortijamiento del cabello
|
Uso
clínico en dermatología
Un
estudio reciente sobre el uso de la AZT en dermatología reveló
que en el UK, las indicaciones más frecuentes fueron las enfermedades
ampollosas, la dermatitis atópica, la dermatitis actínica
crónica y la dermatomiositis. Otros usos comunes incluían
el Hypoderma gangrenosos, el SLE, soriasis, liquen plano y lupus eritematoso
cutáneo.
Guias
terapéuticas:
La
AZT esta contraindicada en pacientes con hipersensibilidad. En los pacientes
con insuficiencia renal o hepática será necesario el ajuste
de la dosis. La medicación no debe ser utilizada durante el embarazo.
No parece producir gonadotoxicidad o infertilidad.
Interacciones
medicamentosas:
No debe ser utilizada conjuntamente con el alopurinol. Los inhibidores
de la ACE parecen potenciar la anemia en pacientes con trasplante renal
tratados con AZT.
La
AZT no deberia utilizarse con el cotrimoxazol ya que podrían tener
un efecto sinergista inhibiendo la proliferación de la médula
ósea.
Dosis
y monitorización
La
azatioprina esta disponible en tabletas de 50 mg (imurel) La dosis inicial
usualmente es de 1-2 mg/kg/día en toma única o dos tomas.
La respuesta terapéutica se observa a las 6-8 semanas. Tras lo cual
puede aumentarse la dosis en intervalos de 0.5 mg/kg cada 4 semanas, sin
superar nunca los 3 mg/kg/día. Si no existe respuesta terapéutica
en 12-16 semanas debe abandonarse la medicación.
|
Guías
terapéuticas en el uso de la AZT
|
|
|
Test
a monitorizar
|
Frecuencia
|
Guias
para modificar la dosis
|
|
|
2.Urea, creatinina
3.Pruebas de función hepática |
1: Semanalmente durante
4 semanas, luego cada 15 días un mes y luego mensualmente
2
y 3:mensualmente |
Reducción de la dosis si existe una
leucopenia menor de4000, o plaquetopenia menor de 100000. suspender la
medicación si la leucopenia es menor de 2500
|
Lear
JT. English JSC, Jons P. Smith AG. Retrospective review of the use of azathioprine
in severe atopic dermatitis. JAAD
35 (4):642-4, 1996
Métodos: Se estudian 35 pacientes con
dermatitis atópica que había recibido azatioprina.
Resultados
35 pacientes (24 varones, 11 mujeres) edad
media:31 a, (5-70); duración media de la AD: 12 años (1-40 años)
dosis: 50 mg/12 horas, duración media 7
meses (1-21 mes)
8/35 (22,9%) tuvieron efectos secundarios
1.3 nausea y epigastralgias severas que
obligaron a suspender el tratamiento
2.5 nausea moderadas
3.Ningún paciente tuvo alteraciones en su
hemograma
En el año siguiente al tratamiento los
pacientes
1.Recibenmenos tandas de antibióticos
2.Menos ingresos hospitalarios
3.Menos visitas ambulatorias
La respuesta al tratamiento fue la siguiente
1.3 (8,6%) tuvo poco efecto
2.18 (69,2) respondieron en el primer mes y en
2 pacientes se requirieron 6 meses para obtener respuesta
La valoración por parte de los pacientes
fue la siguiente (0-10) media: 6,9. 18(de 26:61,5%) pacientes creen que la
mejoría duró hasta 12 meses después de dejar de utilizar el tratamiento
Dado que la azatioprina es más fácil de
monitorizar y mucho más económica, puede ser preferible como tratamiento
sistémico de primer uso en pacientes con dermatitis atópica severa refractaria
a otros tratamientos.
|
Buckley
Da, Baldwin P. Rogers S. The use of azathioprine in severe adult eczema.
JEADV 11 (1998) 137-49
10
pacientes tratados con azatioprina a dosis de 0,7-2,5 mg/kg día
durante un período mínimo de 12 meses fueron evaluados en
u estudio retrospectivo.
8
pacientes mostraron una mejoría importante, pero 3 de ellos se hicieron
refractarios al tratamiento con posterioridad
1
paciente mostró el desarrollo de un linfoma 8 meses después
de dejar el tratamiento.
Los
pacientes fueron 5 varones y 5 mujeres con una edad media de 39.7 años
(28-56) y con una duración media de tratamiento de 15 meses (1-7
años).
§5
pacientes tuvieron una respuesta excelente, requiriendo solo emolientes
y ocasionalmente esteroides tópicos para controlar su enfermedad
y 4 de ellos se mantuvieron en remisión tras un seguimiento de 3
años. Uno de los pacientes que tuvo un brote se volvió a
controlar tras administrar de nuevo la azatioprina.
§3
pacientes respondieron inicialmente bien pero tras 18 meses de tratamiento
dejaron de responder y se tuvo que cambiar la medicación
§1
paciente con una dermatitis atópica fotoexacerbada mejoro sensiblemente
permitiendo una reducción de la dosis de corticoides, pero persistiendo
el eczema en la cabeza y cara.
§El
ultimo paciente tenia una mala respuesta tras 15 meses de azatioprina,
y tuvo que ser cambiado a ciclosporina.
Se
observaron los siguientes efectos secundarios
-linfopenia
transitoria en 3 pacientes
-elevación
de las gama GT en un paciente
-un
paciente desarrollo HSV labial y letargia
El
efecto secundario más importante fu en un varon de 50 años
con unas IgE de 6860 u/ml y con unas VSG persistentemente elevadas (70-100
mmHg) y una anemia microcitica hipocromica que habia sido muy estudiada
antes de administrarles la azatioprina. . El paciente tuvo una respuesta
excelente a la azatioprina, pero posteriormente desarrolló un linfoma.
Snow
JL, Gibson LE. A pharmacogenetic basis for the safe and effective use of
azathioprine and other thiopurine drugs in dermatologic patients. JAAD
1995:32: 114-6.
La
enzima TPMT es clave en el metabolismo tiopurinico así como su papel
en el desarrollo de mielosupresión. La medición de la actividad
de la TPMT facilita las bases para identificar a los pacientes con déficit
de esta enzima, tanto a aquellos con marcado déficit con riesgo
de una mielosupresión marcad- como a aquellos con déficit
parcial.
La
TPMT pude ser determinada en lisados de hematíes y su nivel se relaciona
bien con la actividad hepática.
La
azatioprina se convierte rápidamente a 6 mercaptopurina, la cual
se metaboliza por medio de 3 vías enzimáticas competitivas.
La TPMT cataliza la S-metilización y la xantina oxidasa la oxidación
a metabolitos inactivos. La HGFRT cataliza la conversiónde
las 6 mercaptopurina a 6 tioinosina 5 monofosfato y al nucleotido activo
biológicamente6 tioguanina.
Los
déficits genéticos de XO y de HGFRT son raros, sin embargo
un polimorfismo genético controla la actividad de la TPMT en los
tejidos humanos. El 88,6% son homocigotos para un alelo de la TPMT de gran
actividad, el 0,3% son homocigotos para un alelo de baja actividad y el
11,1% son heterocigotos. Los pacientes con baja actividad tienen riesgo
de una mielotoxicidad severa incluso a dosis bajas de AZT debido a un exceso
de acumulación del metabolito activo de la 6 tioguanina.
También
se ha notado una relación inversa entre la actividad de la TPMT
y la eficacia clínica. Los pacientes en el rango alto de la actividad
de la TPMT (Todos los TPMT homocigotos) tienen a tener una pobre respuesta
clínica comparada con los de rango de baja actividad y con los heterocigotos.
La
medición de los niveles eritrocitarios de TPMT tiene gran importancia
para todos los pacientes tratados con AZT. La determinación de los
niveles basales, preterapéuticos de TPMT, debería ser rutinario
en la práctica ya que teóricamente protegería a 1
de cada 300 homocigotos de una mielosupresión severa y haría
que en esos pacientes la administración de estos medicamentos se
realizase a dosis muy bajas y con un control hematológico cuidadoso.
La determinación del estado heterocigoto llamará la atención
sobre la posibilidad de mielosupresión y en aquellos pacientes con
un rango de actividad de TPMT alto también permitiría la
utilización de dosis más altas.
Snow
JL, Gibson LE. The role of genetic variation in thiopurine methyltransferase
activity and the efficacy and/or side effects of azathioprine therapy in
dermatologic patients. Arch Dermatol 1995 Feb;131(2):193-7
La
tiopurina metil transferaa (TPMT) es uno de los 3 enzimas involucrados
en el metabolismo de la azatioprina y su metabolito activo la 6-mercaptopurina.
La actividad de la tiopurina metiltransferasa está determinada por
un polimorfimo alélico en niveles altos (TPMTH) o bajos (TPMTL).
Los homocigotos para la baja alelos de baja actividad tienen mayor riesgo
de una mielosupresión importante con azatioprina. Los heterocigotos
presentan riesgo de mielosupresión. Los homocigotos para la actividad
alta pueden recibir dosis inadecudamente bjas para conseguir la inmunosupresión
con las dosis convencionales empíricas- de azatioprina. Nosotros
analizados la actividad eritrocitaria de la TPMT y deternimanos los genotipos
de TPMT (basados en el screening de la población normal) en 28 enfermos
dermatológicos. Esta información la correlacionamos con la
eficacia obsevada y los efectos secundarios del tratamiento con azatioprina.
Observaciones:
2 pacientes con niveles inferiores a 12,5 U/mLen
hematíes (ambos TPMTH heterocigotos) mostraron una leucopenica (leucocitos
< 4x10(9)/L) con dosis de azatioprinade
alrededor de 1.5 mg/kg. Un tercer paciente que desarrolló una leucopenia
tenía unos niveles de TPMT en margen inferior del rango homocigoto
(15.5 U/mL) pero reibio dosis más altas(2.6mg/kg)
que el resto de pacientes en la serie. 10 pacientes con niveles de TPMT
de más de 18.5 U/mL(todos
TPMTH homocigotos)recibiendos dosis menores de 1.5 mg/kg de azatioprina
se valoró que tenían una respuesta pobre al tratamiento.
En comparación 7 pacientes con niveles entre 12.5 y 18.5 U/ml (6
TPMTH homocigotos y 1 TPMTH heterocigoto) recibiendo dosis de entre 0.9
y 1.8 mg/kg de azatioprina tuvieron una respuesta clínica beneficiosa.
Los efectos secundarios gastrointestinales y los tests de función
hepática no parecen correlacionarse con la actividad de TPMT.
Conclusión:
Los pacientes TPMTH heterocitos pueden tener un riesgo elevado de mielosupresión
con las dosis altas empíricas de azatioprina. Por otro lado los
TPMTH homocigotos especialmente aquellos en los rangos altospueden
tener una respuesta clínica inadecuada a las dosis utilizadas de
forma empírica
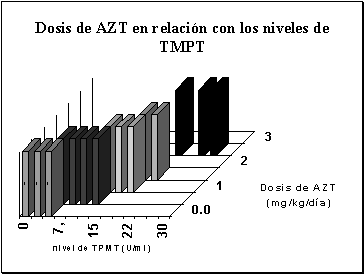
|
Dosis de azatioprina en relación a los niveles hemáticos
de TPMT
|
|
|
|

|
Scerri
L. Azathioprine in dermatológica practice. An overview with special
emphasis on its use in non-bullous inflammatory dermatosis. Adv Exp Med
Biol 1999, 455:343-8.
Hemos realizado un estudio retrospectivo
para observar el uso de la azatioprina como monoterapia en dermatosis inflamatorias
no ampollosas. Estudiamos un total de 24 pacientes (10v/14M). Las dermatosis
incluian dermatitis atópica (10), pompholix (6), psoriasis en placas
(6) y dermatitis actínica crónica (2). Todos los pacientes
tenían una enfermedad severa y refractaria que hacia preciso la
utilización de una medicación sistémica de segunda
línea. La edad media fue de 49,4 años (17-86ª). La dosis
inicial de azatioprina fue de 100-150 mg/dia y la dosis de mantenimiento
de 50-100 mg/dia. La duración media del tratamiento fue de 33,5
meses (1-132 meses). 18 pacientes (75%) mostraron una respuesta buena y
excelente a la azatioprina. La mejoría se observo en las 4 dermatosis
estudiadas. Las reacciones adversas encontradas fueron elevación
de la VCM (6), leucopenia (2), elevación de enzimas hepáticos
(6) y dispepsia (4). La medicación se suspendió en 2 pacientes
debido a los efectos secundarios (dispepsia y elevación de enzimas
hepáticas) que se normalizaron. Otros factores que potencialmente
pueden contribuir a los efectos secundarioa observados estaban presentes
en 5 pacientes y fueron alcoholismo (2) intoxicación por eritromicina
(1) y malabsorción (2). Nuestro estudio demuestra la eficacia de
la azatioprina como monoterapia de la dermatitis atópica severa,
pompholix, psoriasis en placas y dermatitis actínica crónica.
Aun más la azatioprina es una medicación de bajo oste y por
lo general es bien tolerada.
Tan
BB y col Azathioprine in dermatology: A survey of current practice in the
UK. Br. J
Derma 1997 136:351-5.
La
azatioprina tiene un papel importante enel
tratamiento de varias dermatosis inflamatorias. Nosotros realizamos una
encuesta sobre el uso actual de la azatioprina entre los dermatólogos
en el reino unido. El índice de respuestas fue del 68%. A diferencia
de las instrucciones del fabricante, la AZT se utiliza en varias dermatosis.
Las entidades mas frecuentemente tratadas fueron penfigoide, penfigo y
dermatitis atópica.Además
encontramos que solo un 13% de los dermatólogos prescribían
la azatioprina en relación con el peso. La mayoría de los
dermatólogos creían que la azatioprina es una medicación
bien tolerada. Ninguno realizaba medicaciones de la TPMT, que se supone
que es un buen indicador de la mielosupresión. La utilización
de la dosis en relación con el peso y las mediciones de TPMT será
una forma de optimizar la utilización de la azatioprina.