Infecciones bacterianas cutáneas
Introducción
Una de las funciones más importantes de la piel es su acción barrera frente a la
invasión y crecimiento de los agentes infecciosos patógenos.
Resistencia natural de la piel: la piel intacta es muy resistente
a la invasión de una gran variedad de bacterias, a las cuales esta
constantemente expuesta. Es difícil producir infecciones localizadas
tales como el impétigo, forunculosis y/o celulitis en los animales
de laboratorio o en voluntarios sanos. Los diferentes factores que influyen
en la resistencia cutánea a las infecciones están resumidos
en la tabla 1.
Patogénesis de las infecciones bacterianas
cutáneas: El establecimiento de una infección cutánea
depende de la relación entre el organismo y el huésped (piel),
esta relación bacteria-huésped, depende en gran medida de
tres factores:
-
La integridad cutánea como resistencia natural de la piel a las
infecciones, determinada por los factores resumidos en la tabla 1.
-
Propiedades patogénicas del organismo: La capacidad de producir
infección depende:
-
a) de la capacidad invasiva del organismo y de la
respuesta inflamatoria que produce y
-
b) de las propiedades toxigénicas del mismo.
-
Respuesta inflamatoria: A pesar de las escasas variaciones en relación a las células inflamatorias
presentes en la piel, existen diferentes patrones clínicos y morfológicos en las
infecciones cutáneas, generalmente dependientes de la localización de la
infección. En relación a la presentación clínica y estructura cutánea afecta se
clasifican las infecciones cutáneas en impétigo, ectima, celulitis, fasceitis
necrotizante, foliculitis, forúnculosis, antrax, etc(Tabla 2).
-
Propiedades toxigénicas del organismo, que pueden tener
un efecto directo en el tejido o actuar como superantígenos.
|
Tabla 1
Factores que influyen en la resistencia natural de
la piel a las infecciones
|
-
pH bajo, temperatura baja
-
Presencia de sustancias antibacterianas naturales
peptidos antimicrobianos endógenos
-
Factores de inmunidad celular y humoral
-
Sequedad relativa de la piel
-
Interferencia bacteriana
|
|
|
Métodos diagnósticos: La identificación del agente causal de las
infecciones cutáneas se realiza, al igual que en infecciones en otras
localizaciones, por medio de:
-
Examen tras tinción: La tinción de
gram
permite visualizar lo morfología del agente infeccioso y permite diferenciar
entre bacterias gram + (teñidas de color violeta) y bacterias gram - (teñidas de
color rosa).
-
Por medio de la realización de cultivos
bacteriológicos (tanto de los exudados como de las biopsias cutáneas).
-
Determinación de antígenos bacterianos: permiten
detectar los antígenos microbianos en las muestras mediante la utilización de
anticuerpos específicos utilizando técnicas como la aglutinación, enzima-inmunoanálisis,
inmunofluorescencia, PCR, etc
Infecciones por Streptococcus pyogenes.
Los estreptococos son un grupo heterogéneo de bacterias que causan
diferentes cuadros clínicos. Son cocos Gram+, que se disponen
en parejas o cadenas de longitud variable. El Streptococcus pyogenes,
(grupo
A de la clasificación de Lancefield) es un microorganismo que puede
encontrarse formando parte de la flora de las vías respiratorias superiores y en
determinadas zonas húmedas y calientes de la superficie cutánea. En ocasiones es capaz de producir infecciones
cutáneas y de otras localizaciones (faringoamigdalitis, neumonía,
sepsis puerperal e infecciones del recién nacido). Además
de los diferentes procesos supurativos puede provocar cuadros post-infecciosos
de base inmune, especialmente la fiebre reumática y la glomerulonefritis
postestreptocócica. La diferente invasividad y agresividad entre
las cepas saprófitas y cepas patógenas se basa en el estado
inmunitario del huésped y en las características del microorganismo.
La virulencia del S. pyogenes depende en gran medida de la proteína
fibrilar presente en su pared, denominada proteína M, de la cual
se conocen al menos 80 tipos y también de la capacidad de producción
de toxinas, entre las que destacan la estreptolisina S y O, y las
toxinas pirogénicas (A, B y C) que son responsables de cuadros
sistémicos como la escarlatina, fasceitis necrotizante y síndrome
de shock tóxico estreptococico. Los cuadros clínicos cutáneos
producidos por el S. pyogenes están resumidos en la tabla
3.
|
Tabla 3
Infecciones cutáneas producidas por S. pyogenes
|
|
Tipo de lesión |
Localización |
Presentación clínica |
Hallazgos asociados |
|
Impétigo
contagioso |
Áreas expuestas |
Lesiones vesiculosas
que evolucionan a costras |
Puede desarrollarse
tras pequeños traumatismos o picaduras, puede ser pruriginoso o
doloroso. Linfadenopatía regional. |
|
Ectima |
Extremidades inferiores |
Ulceras en sacabocados
cubiertas de costra amarillenta que se extiende hacia la dermis adyacente |
Tras traumatismos |
|
Erisipela |
70-80% en extremidades
inferiores
5-20% en cara |
Placas rojas e induradas
de márgenes llamativos |
Fiebre y leucocitosis, |
|
Celulitis |
Extremidades inferiores
y superiores, tronco, glúteos, cara |
Lesiones eritemato-edematosas
con o sin borde elevado |
tumefacción
local, dolor, eritema, mal estado general, escalofríos, linfadenopatia
regional |
|
Celulitis perianal |
región perianal en pacientes pediátricos |
Placas eritematosas bien delimitadas |
Dolor local |
|
Fasceitis
necrotizante |
Extremidades inferiores.
Región genital. Áreas de traumatismo o intervenciones previas |
Placas eritemato-edematosas
que evolucionan hacia ampollas y gangrena |
Fiebre, mal estado
general, leucocitosis |
|
Dactilitis
estreptococica |
Pulpejo de dedos |
Lesiones vesículo-ampollosas |
Dolor local |
-
Pioderma superficial: Es un término con el cual se
describe cualquier infección superficial de la piel ocasionada por
bacterias.
-
Impétigo (Impétigo
contagioso): Infección cutánea inicialmente vesicular, que
evoluciona hacia costra, causada generalmente por estreptococos del grupo
A, con frecuencia en el impétigo contagioso también pueden aislarse
estafilococos en combinación con el streptococo o de forma aislada.
El impétigo es una infección contagiosa que afecta especialmente
a niños en edad preescolar. Es más frecuente en verano y
otoño. Tras la adquisición del estreptococo en la piel normal,
a partir de un contacto cercano, el desarrollo de traumatismos menores
predispone al desarrollo de la infección cutánea. Cuando el
impétigo aparece sobre una lesión cutánea previa recibe el nombre de
impetiginización. El proceso
inflamatorio del impétigo es superficial, con una vesiculo-pústula
unilocular, localizada por encima del estrato granuloso, que en el curso
de los días evoluciona hacia la formación de una costra melicélica.
Los pacientes con impétigo pueden desarrollar una discreta leucocitosis.
El estudio de Gram del contenido de una vesícula va a revelar la
existencia de cocos Gram positivos. Él diagnóstico generalmente
no plantea problemas cuando las lesiones se observan en el estadio de costra.
Si no se trata las lesiones van apareciendo progresivamente durante semanas.
El tratamiento local, con limpieza de las costras es muy útil. En
casos leves el impétigo contagioso se trata mediante la aplicación
tópica de mupirocina al 2%. En casos más complicados y extensos
es aconsejable utilizar antibióticos orales como amoxi-clavulánico
o cefalosporinas
-
Impétigo y glomerulonefritis post estreptococica:
La glomerulonefritis postestreptocócica es una complicación
no supurada de una infección cutánea y con menor frecuencia
faríngea, causada por cepas nefritogénicas del streptococcus.
La incidencia es desconocida ya que muchos casos son asintomáticos.
La glomerulonefritis postestreptocócica (GMNPS) se desarrolla
10-15 días después de la infección aguda con hallazgos
clínicos de una GMN aguda, con hematuria macroscópica, oliguria,
insuficiencia renal, edema e hipertensión. Afecta predominantemente
a niños de entre 2 y 10 años. El mecanismo de producción
no está bien establecido, existiendo datos que sugieren el depósito
de inmunocomplejos o el depósito a nivel glomerular de antígenos
estreptocócicos (endostreptosina, proteínas nefríticas,
etc) con la siguiente producción de anticuerpos que se unirían
a los antígenos depositados a nivel glomerular. El hallazgo analítico
más característico de las infecciones estreptocócicas
de vías respiratorias es la presencia de anticuerpos antiestreptolisina
O (ASLO), por contra tras una infección cutánea los ASLO
suelen estar normales mientras que existe una elevación de los títulos
de anti-DNAasa B y antihialuronidasa. Al menos el 90% de los pacientes
con GMNPS tienen niveles elevados de anti-DNAasa, sugiriendo que la fuente
de la cepa nefrítica se localice en un pioderma. La GMNPS suele
tener un curso benigno con resolución espontánea y relativamente
rápida de los síntomas.
-
Escarlatina: Cuadro clínico que puede
acompañar a ciertas infecciones estreptocócicas especialmente la
faringoamigdalitis. Es debido a la producción de la toxina eritrogenica de
la cual existen tres tipos A, B y C, siendo el A el que se relaciona con
mayor gravedad. La escarlatina afecta especialmente a niños cursa con
un exantema rojo brillante, de inicio en torax, que posteriorment se
extiende a tronco y cuello. Se afectan más los pliegues axilares, inguinales
coincidiendo con los pligues normales (líneas de Pastia)
-
Ectima: lesión es semejante al impétigo, se
inicia de la misma manera pero la lesión se extiende de forma más
profunda para producir una úlcera superficial. Las lesiones suelen
localizarse en las extremidades inferiores de los niños o ancianos
tras traumatismos superficiales.
|
Factores de riesgo para el
desarrollo de celulitis e infecciones de tejidos blandos |
-
Traumatismos (laceraciones, quemaduras,
abrasiones, fracturas abiertas)
-
Mordeduras (animales o humanas)
-
Adicción a drogas intravenosas
-
Situaciones con predisposición a infecciones:
diabetes, insuficiencia arterial, linfedema, insuficiencia
renal, cirrosis, neutropenia e hipogamaglobulinemia
-
Historia de celulitis estreptocócica previa
(especialmente si existe tiña pedis previa)
-
Mastectomia radical con disección axilar
-
disección de la vena safena
|
-
Erisipelas:
infección superficial con afectación de los tejidos profundos,
es una celulitis superficial con marcada afectación linfática,
generalmente producida por el estreptococo grupo A.
La erisipela se observa
con frecuencia en los niños y adultos. Los factores predisponentes
en los adultos son el enolismo, diabetes, inmunosupresión, cicatrices
quirúrgicas recientes o antiguas con obstrucción linfática o venosa. Las lesiones se inician con una pequeña herida en la piel
que posteriormente no es detectable. Las lesiones cutáneas tiene
un aspecto eritematoso indurado, que adopta la morfología de la
piel de naranja, extendiéndose por la periferia con un margen ligeramente
sobreelevado en el cual pueden observarse ocasionalmente vesículas.
La localización característica es la afectación del
dorso de nariz y mejillas donde adopta el aspecto en alas de mariposa sin
embargo, en la actualidad el porcentaje más alto de casos se localiza
en las extremidades inferiores produciéndose a partir de lesiones
banales como una tiña pedis interdigital. Los pacientes afectos
pueden presentar fiebre, mal estado general y alteraciones analíticas
como elevación de la VSG, leucocitosis de más de 15000 cel
/mm3, los hemocultivos son positivos en un escaso número
de pacientes. Las lesiones suelen responder rápidamente a la administración
de antibióticos sistémicos (penicilina o eritromicina). Los
pacientes con lesiones originadas a partir de una tiña pedis interdigital deben
recibir tratamiento de la misma.
-
Celulitis: La celulitis es una infección aguda de la dermis y tejidos
subcutáneos que generalmente aparece como complicación de una herida, úlcera o
dermatosis previa, raramente son causadas por una infección subyacente (osteomilitis)
o una bacteriemia (en pacientes diabéticos o inmunodeprimidos). Suele
localizarse en la pierna que se encuentra eritemato-edematosa, dolorosa y
caliente al tacto, careciendo del borde sobreelevado y del aspecto en piel de
naranja que caracteriza a la erisipela o celulitis superficial. Existen diversas
formas clínicas de celulitis que están en relación a su localización y
factores predisponentes. El diagnóstico se basa en las características clínicas
de la misma, puede realizarse un cultivo de aspirado o de biopsia pero no suelen
ser necesarios. los hemocultivos suelen ser negativos. Los estudios radiológicos
pueden ser útiles para diferenciar una celulitis de una fasceitis necrotizante.
Existe una forma especial de celulitis que afecta a niños, causada por el S.pyogenes, caracterizada por el desarrollo de eritema perianal, dolor en la
defecación y presencia de sangre en heces.
-
Fasceitis necrotizante:
La fasceitis necrosante es una infección
aguda y grave de los tejidos subcutáneos profundos y de la fascia,
sin supuración evidente, pero con gran necrosis del tejido graso
y fascia y que puede ser mortal si no se reconoce pronto y no se instauran
tratamientos quirúrgicos y antibioticos precoces.
|
Hallazgos clínicos que sugieren una fasceitis
necrotizante |
-
Crecimiento rápido del área de infección
-
Desarrollo de ampollas violáceas
-
Coloración rojo purpúrica de la piel
-
Induración leñosa de la zona infectada
-
Desarrollo de áreas pálidas en las zonas infectadas
-
Dolor
o tumefacción desproporcionada para la presentación de celulitis
-
Manifestaciones sistémica toxicas
-
Síndrome séptico
|
Se caracteriza
por una rápida y extensa necrosis, que se extiende por los planos
de las fascias, para afectar posteriormente a la piel y los tejidos subyacentes
y se acompaña de signos de toxicidad sistémica. La necrosis
se localiza en un principio en la grasa subcutánea, fascia
y la piel, respetando el músculo. En etapas avanzadas se puede afectar
el plano profundo muscular produciendo marcada rabdomiolisis. La fasceitis
necrotizante se divide fundamentalmente en dos tipos, el tipo 1 (80% de casos) causado
por flora anaerobia mixta, con bacilos aerobios gram-negativos y cocos gram-positivos
y el tipo 2 (20%) causado por el estreptococo del grupo A. El tipo 1 tiene varias
formas especiales dependiendo de la localización, que están
resumidas en la tabla 4. El diagnóstico de la fasceitis necrotizante debe
establecerse de forma rápida, clínicamente el cuadro se inicia con dolor
intenso, acompañado de signos inflamatorios escasos. El aspecto clínico de las
lesiones cutáneas en las primeras 24-48 horas es de eritema e hinchazón y sólo
es patognomónico entre el segundo y el cuarto día, con la aparición de áreas
azuladas y vesículas violáceas. El tratamiento debe iniciarse de forma temprana
y ser agresivo fundamentándose en la cirugía, antibióticos y vigilancia de las constantes vitales.
Es necesaria la escisión y la limpieza agresiva de todos los tejidos necrosados, tanto piel, tejido subcutáneo o fascia con desbridamiento,
fasciotomía, escisión y amputación tempranas si procede
La Fasceitis necrotizante tipo 2, producida por el estreptococo
grupo A solo o en ocasiones acompañado de Staphylococus aureus
o
epidermidis
es una infección infrecuente de los tejidos subcutáneos y
de la fascia, que progresa rápidamente con necrosis y produce síntomas
sistémicos graves. Se desarrolla generalmente en las extremidades
tras un traumatismo o lesión previa, desde heridas profundas, heridas
quirúrgicas y hematomas, hasta lesiones triviales o erupciones por
varicela o pequeñas lesiones cutáneas banales como un arañazo
o un corte. En la fasceitis necrotizante existe una rápida destrucción
de la grasa y fascia, con necrosis y licuefacción , infiltrado de
polimorfonucleares y trombosis de los pequeños vasos. La clínica
se caracteriza por un inicio rápido de dolor intenso, hinchazón
y eritema con una extrema sensibilidad al tacto. La parte afectada suele
presentar un color rojo característico y extenderse rápidamente
las primeras 24-48 horas. La infección evoluciona velozmente con
signos tóxicos importantes, escalofríos, taquicardia y fiebre
alta. Hay una disociación entre el aspecto sano de la piel y uno
dolor muy intenso. La virulencia de la infección por estreptococo
en la fasceitis necrotizante se debe a factores locales de la infección
como la presencia de proteínas de superficie que facilitan la adherencia
e invasión y también por la producción de exotoxinas
que tienen efecto local y sistémico al actuar como superantígenos.
El diagnóstico de la fasceitis necrotizante es fácil de establecer
en los estadios finales, sin embargo en su inicio debe plantearse el diagnóstico
diferencial entre celulitis y fasceitis necrotizante, siendo esta diferencia
de extrema importancia ya que la celulitis responderá al tratamiento
antibiótico mientras que la fasceitis necrotizante requiere un
tratamiento
quirúrgico agresivo y amplio además de la utilización
de antibioticoterapia adecuada.
La
fasceitis necrotizante tipo III no está aceptada de forma generalizada, está
causada por Vibrio vulnificus. Se adquiere a través de heridas y tras
el contacto con agua de mar templada, siendo más frecuente en las
zonas costeras y en pacientes con infección por hepatitis B crónica. Si bien
es la forma menos frecuente de fasceitis necrotizante, presenta un curso
fulminante y debe ser reconocida precozmente para realizar una intervención
quirúrgica.
|
Tabla 4
Clasificación de las fasceitis necrotizantes |
|
tipo |
Agentes etiológicos |
Factores predisponentes |
Manifestaciones clínicas |
|
Fasceitis necrotizante tipo
I |
Flora anaerobia mixta, bacilos
gram negativos, estreptococos, |
cirugía, diabetes mellitus,
enfermedad vascular |
Afectación de grasa y fascia. |
|
Formas especiales |
|
Gangrena sinérgica de
Meleney |
Aparece tras cirugía abdominal como una ulceración
superficial limitada a la fascia superficial, con necrosis y dehiscencia de la
herida |
|
Gangrena de Fournier |
celulitis que afecta a fascia del escroto, periné y
órganos sexuales |
|
Gangrena sinergistica
progresiva bacteriana |
suele aparecer tras una intervención quirúrgica,
colostomias, ileostomias o úlceras tórpidas. Suele acompañarse de escasa
afectación sistémica |
|
Fasceitis necrotizante tipo
II |
Streptococcus pyogenes (grupo
A) solo o en ocasiones acompañado de staphilococcus aureus
o epidermidis |
traumatismo previo, cirugía,
diabetes, venopunción, enfermedad vascular periférica |
Inicio brusco con dolor intenso,
fiebre y mal estado general y afectación multiorgánico |
|
fasceitis
necrotizante tipo III |
vibrio vulnificus |
hepatitis B crónica |
shock fulminante en las fases precoces de la infección. |
|
bmj 2012 practice pointer. necrotizing fasciitis |
Síndrome del Shock tóxico estreptococico:
Consiste un un cuadro grave con toxicidad sistémica, shock séptico,
eritema macular y fallo multiorgánico, con elevada mortalidad, y
que se denominó así por su similitud al síndrome del
shock tóxico estafilocócico. El síndrome se relaciona
habitualmente con una infección de tejidos blandos, el 70% de los
pacientes tienen una fasceitis necrotizante. En el 60% de los pacientes se
observa una puerta de entrada al nivel de piel o mucosas y en el resto es
posible que se deba a una infección profunda o tras una bacteriemia originada
en la faringe. La primera fase inicial consisten
en mal estado general, mialgia, escalofríos, fiebre, vomito y diarrea.
Tras esta fase se pasa a una segunda fase de taquicardia, fiebre, taquípnea
y dolor en la zona de infección. En la fase 3 persiste la fiebre
y se desarrollan signos de shock y afectación de órganos.
Estudios epidemiológicos han relacionado el síndrome de shock
tóxico estreptococico con cepas del serotipo M1 y 3, estas cepas
producirían exotoxinas, entre las que destacan la speA, speB, y
speC y hemolisinas, estreptolisinas O y S, hialorunidasa, ADNasa y
estreptocinasa.
La toxina speA es producida por un 85% de los estreptococos del grupo A
aislados en el síndrome del shock tóxico. Existen evidencias
de que las manifestaciones del síndrome del shock tóxico
estreptococico son debidas a superantígenos (Tabla 5). La speA produce
una estimulación masiva y no específica de la proliferación
de células T. La activación de un gran número de clonas
de linfocitos T hace liberar de foma masiva citocinas: TNF, IL-1, IL2,
e INF-gamma. Las citocinas de forma directa o indirectamente a través
de la inducción de una segunda oleada de mediadores y sustancias
proinflamatorias conducen al síndrome de respuesta inflamatoria
sistémica y al fallo multiorgánico. En los últimos
años se está reconociendo la participación de los superantígenos no solo en este cuadro y relacionados -fasceitis
necrotizante, síndrome del shock tóxico estreptocócico,
shock tóxico estafilocócico- sino que además se está
expandiendo su participación en diferentes patologías tales
como la enfermedad de
Kawasakil (síndrome ganglionar mucocutáneo),
síndrome descamativo recurrente y el eritema
perineal recidivante mediado por toxinas. Recientemente se ha demostrado en
animales que la proteína
M presente en la pared de los estreptococos tendría también un papel clave
en la patogenia del síndrome del shock tóxico
estreptocócico.
|
Tabla 5. Mecanismo de activación del superantígeno
|
|
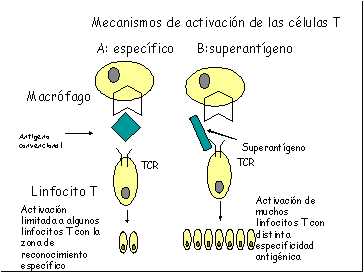 |
Mecanismo de acción
de un superantígeno: A la izquierda (fig A) la célula
presentadora (monocito macrófago) expone a través de las
proteínas del complejo mayor de histocompatiblidad (MHC) el antígeno
al receptor del linfocito T (TCR). Este TCR reconoce específicamente
la configuración de un antígeno específico y se activa
un número escaso de células T: las que poseen el receptor
de dicho antígeno. A la derecha (Fig B), las toxinas estreptococicas
se unen al MHC y al TCR no en las zonas de reconocimiento específico,
sino en las adyacentes, y se activan numerosísimas clonas de distinta
especificidad antigénica, esta actividad se conoce como superantígeno.
La activación por el mecanismo de los superantígenos puede
activar entre el 5% y el 30% de toda la población de células
T, mientras que el mecanismo de activación por medio de antígenos
convencionales activa entre el 0,01% y el 0,1% de las células T. |
|
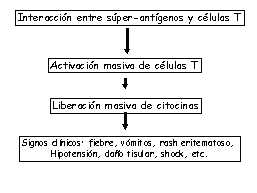 |
La activación de gran número
de células T por parte de los superantígenos produce una
liberación masiva de citocinas (factor de necrosis tumoral alfa,
interleucina 1, e interleucina 6, que producen una serie de síntomas
clínicos como la fiebre, rash, vomitos, hiptensión, shock,
etc. |
Infecciones por Staphylococcus Aureus
El S. Aureus es miembro de la familia de los micrococos, es gram
positivo, se dispone en racimos o grupos y el cultivo adquiere una
coloración blanquecina-dorada que le confiere el nombre. El S.Aureus
tiene
un gran potencial patogénico debido a la gran cantidad de toxinas
y enzimas que es capaz de producir como la citotoxina (toxina de bajo peso
molecular que induce la lisis de numerosas células y marcada inflamación),
la enterotoxina (con actividad como superantígeno, involucrada en
el síndrome del shock tóxico y en las toxiinfecciones alimentarias),
la toxina epidermolítica ( que produce eritema cutáneo y
separación epidérmica, involucrada en el síndrome
de la piel escaldada). Los principales cuadros clínicos cutáneos
están resumidos en la tabla 6.
|
Tabla 6
Infecciones cutáneas producidas por S. aureus
|
|
Tipo de lesión
|
Localización
|
Presentación clínica
|
Hallazgos asociados
|
|
Impetigo
ampolloso |
Extremidades, tronco, pliegues |
Máculas eritematosas con
vesículas, signo de Nikolsky positivo |
Signos inflamatorios locales
adenopatía |
|
Síndrome de la piel escaldada
estafilococica |
extensa |
grandes ampollas y exfoliación
de toda la superficie cutánea |
fiebre, postración general |
|
Foliculitis |
Folículos pilosos, regiones
apocrinas |
Pápulas eritematosas cubiertas
de una pústula central |
Prurito |
|
Forúnculo |
Cara, cuello, axila, glúteo |
Nódulos profundos, inflamatorios |
Dolor |
|
antrax |
Base de cuello, espalda, muslos |
Lesiones induradas más
profundas que el forúnculo e intercomunicadas |
Fiebre malestar general |
|
Botriomicosis |
Etiologia: Stpah aureus, también P aeruginosa, E coli, Proteus |
Nódulos o placas supurativas en cualquier localización |
Pacientes inmunodeprimidos (HIV), dbtes, traumatismos, alcoholicos |
|
Hidrosadenitis supurativa |
axilas, ingle, cuello, glúteo |
nódulos inflamatorios fistulizados |
dolor y supuración local |
|
Paroniquia aguda |
pliegue ungueal |
Inicio brusco de placa eritematosa,
fluctuante y purulenta |
dolor al tacto |
-
Impétigo ampolloso: Infección causada por el
estafilococo aureus grupo Fago II. En el pasado el estafilococo áureos
solo representaba la causa del 5-10% de los casos de impétigo, pero
su frecuencia está en aumento. El impétigo ampolloso se observa
principalmente en los recién nacidos y se caracteriza por la rápida
progresión de vesículas hacia ampollas flácidas. Las
ampollas contienen serosidad blanco amarillenta.
-
Síndrome
de la piel Escaldada por Estafilococo (SSSS o Síndrome de Ritter
von Rittershain): Esta es la forma más severa de infección
cutánea debida a la exotoxina exofoliativa producida por el estafilococo
áureos del grupo fago II tipos 71 y 55. Se caracteriza por la formación
de ampollas generalizadas y exfoliación extensa. A diferencia de
el impétigo ampolloso, en las lesiones cutáneas no es posible
encontrar el estafilococo que estará en una infección cutánea
o en otra localización (nasofaríngea o conjuntival). Solo
la toxina producida por el fago grupo II es capaz de producir el síndrome.
Las lesiones histológicas se caracterizan por la formación
de una separación epidérmica, al nivel de la capa granular,
con escasa reacción inflamatoria acompañante. El síndrome
de las 4 S (SSSS) generalmente se observa en niños recién
nacidos (Síndrome de Ritter) o en niños un poco más
mayores. Tiene un inicio brusco con eritema difuso, semejante al de la
escarlatina y con un signo de Nikolsky positivo, acompañado de mal
estado general. Se observa la formación de grandes ampollas de contenido
claro que se rompen con extrema facilidad. El mecanismo del síndrome
de las 4S ha sido objeto de debate. En la actualidad existen evidencias
que demuestran que las toxinas exfoliativas A y B producidas por los estafilococos
atacan directamente la proteína desmogleína
1, que está presente en los desmosomas de las células
epidérmicas situadas en los niveles altos de la epidermis. El daño
producido por esta toxina sobre la desmogleína causaría la
separación entre las células epidermicas altas, dando lugar
a la formación de una ampolla subcórnea. El mecanismo de
formación de la ampolla en este caso es similar al mecanismo observado
en el pénfigo foliáceo donde se producen anticuerpos contra
la desmogleína 1.
-
Síndrome del Shock tóxico: consiste en el desarrollo
de un cuadro sistémico causado por la infección por staph
aureus productores de toxinas y caracterizado por fiebre, erupción
eritematosa generalizada y afectación sistémica con hipotensión,
fallo multiorgánico y descamación generalizada siguiendo
un patrón escarlatiniforme. Inicialmente se observó -aunque
no de forma exclusiva- en mujeres en el ciclo menstrual, relacionándose
con la utilización de tampones hiperabsorbentes. El agente causal
más frecuente es el staph aureus productor de la toxina 1 (en el
93% de las mujeres en el ciclo menstrual) o la toxina 2 (62% de casos no
relacionados con el ciclo menstrual). En los últimos años
los casos no relacionados con el ciclo menstrual han aumentado, representando
un tercio de los casos y estando relacionados con infecciones localizadas,
cirugía y picaduras. Las toxinas producidas por el staph aureus
actuarían como superantígenos por medio de la unión
con el complejo mayor de histocompatibilidad produciendo una marcada proliferación
de células T no específica con la liberación de gran
cantidad de citocinas.
-
Foliculitis, forúnculos y antrax: Estas tres entidades
representan una continuidad en lesiones que afectan al folículo
piloso causadas por el S. aureus. La foliculitis se inicia con la
afectación de un solo folículo, con formación de una
vesículo-pustula folicular, rodeada de un halo eritematoso. Se desarrolla
un forúnculo cuando la porción folicular afecta a la dermis
profunda y al tejido subcutáneo. Si se afectan varios folículos
desarrollándose una lesión más grande con múltiples
puntos de drenaje se habla de antrax, desarrollándose estas lesiones
especialmente en pacientes inmunodeprimidos o diabéticos. Debe diferenciarse
el antrax estafilocócico del carbunco (antrax) producido por el
bacillus
antracis.
-
Hidradenitis supurativa: enfermedad crónica, recurrente,
muy molesta que consiste en un proceso infeccioso de las glándulas
apocrinas de la región axilar e inguinal. Generalmente está
causada por el estafilococo áureos, si bien también es frecuente
aislar bacilos gram negativos como el proteus. Clínicamente las
lesiones se manifiestan como nódulos violáceos purpúricos,
que semejan furúnculos y que drenan a la piel a través de
conductos sinuosos.
-
Infecciones cutáneas por S. aureus resitentes a la meticilina (MRSA):
El S. aureus fue la bacteria que desarrolló más rápidamente resistencia a la
penicilina. A partir de los años 60 y tras la introducción de la meticilina se
empezaron a detectar colonias de S.aureus resistentes a este y otros
antibióticos, generalmente eran infecciones nosocomiales y que afectaban a
personas con factores de riesgo tales como dermatosis crónica, cirugía,
cateteres endovenosos, etc, llegando en los últimos años a representar en
nuestro país hasta el 24% de las cepas de S.aureus aisladas en los hospitales.
En la última década se empiezan a detectar casos de infecciones por MRSA
en la comunidad, con unas características microbiológicas y clínicas
diferentes de las infecciones nosocomiales, caracterizándose por una
sensibilidad a un espectro mayor de antibióticos, la producción de la
proteína PVL y por el desarrollo de lesiones clínicas acompañadas de marcada
necrosis. El S. Aureus resistente a la meticilina es en ciertas áreas el
patogeno más frecuente como causante de infecciones cutáneas y de tejidos
blandos. Las lesiones cutáneas se caracterizan por acompañarse de marcada
necrosis semejando lesiones secundarias a picaduras muy inflamatorias. También
se han descrito otras cuadros como neumonia necrotizante, empiema pleural,
fasceitis necrotizante, tromboflebitis séptica con embolización pulmonar,
miositis y sepsis severa con púrpura fulminans y síndrome de Waterhouse-friderichsen.
El tratamiento de las infecciones cutáneas sin afectación sistémica
generalmente se tratan con incisión y drenaje con o sin antibióticos, siendo el
tratamiento quirúrgico suficiente para lesiones pequeñas (<5cm). Estudios
controlados con placebo, sugieren que con la prevalencia de infecciones por
staphylococcus aureus methicillin resistente, el tratamiento de los abascesos
cutáneos no complicados mediantee la incisión y drenaje asociado a tratamiento
antibiótico con trimetroprim-sulfametoxazol o clindamicina, presentan una mejor
evolución.
Infecciones cutáneas por corinebacterium
El corinebacterium es un bacilo Gram+ que afecta con frecuencia a sujetos
que viven en climas húmedos produciendo 3 tipos de infecciones clínicas:
el eritrasma, la queratolisis puntata y la tricomicosis axilar
. El Eritrasma
es una infección superficial, localizada especialmente en pliegues
axilar e inguinal, caracterizada por el desarrollo de placas eritematosas,
bien delimitadas, cubiertas de una fina escama blanquecina. Es característico
que esta lesión adquiera un color rojo-coral en el examen con luz
de Wood. La queratolisis punctata es una infección que afecta
especialmente a plantas y suele afectar a individuos con marcada hiperhidrosis
y bromhidrosis. Se caracteriza por el desarrollo de hoyuelos de tamaños
variables, confluentes que suelen afectar unicamente al estrato córneo.
La tricomicosis axilar es tambien una infección bacteriana superficial
que afecta al vello axilar y menos frecuentemente al púbico. Se
caracteriza por el desarrollo de vainas amarillentas adheridas al tallo
del pelo que son visibles a simple vista y en el examen microscópico
con tinción de Gram puede demostrarse que están consituidas
por agregados de bacilos Gram+.
Infecciones por Pseudomona aeruginosa
La P.aeruginosa es un bacilo Gram negativo, que en medios de cultivo produce
colonias de color azul-verdoso debido a la producción de pigmentos.
Se encuentra ampliamente difundida en la naturaleza en íntima asociación
con medios húmedos. La P.aeruginosa afecta con frecuencia las estructuras
cutáneas produciendo diversos cuadros clínicos como foliculitis,
infecciones ungueales (donde las uñas adquieren un color verdoso
característico), otitis externa, infección del pliegue interdigital e infección de las heridas quirúrgicas.
En pacientes con sepsis por P.aeruginosa se produce una lesión cutánea
característica denominada ectima gangrenoso, que consiste en el
desarrollo de placas duras redondeadas con una escara necrótica
verdosa en su centro que es casi patognomónica de la sepsis por
pseudomona.
|
Infecciones
cutáneas por
Pseudomona aeruginosa
|
|
Tipo de
lesión |
Localización |
Presentación clínica |
Hallazgos
asociados |
|
Foliculitis |
Tronco |
maculas
papulas y pustulas de distribución folicular |
|
|
Infecciones
ungueales |
uñas de manos |
discoloración
verdosa de las uñas |
puede
asociarse a onicomicosis |
|
Infecciones del pliegue interdigital |
Pliegue
interdigital de los pies |
maceración y
fisuras en el pliegue interdigital |
Se observa en
pacientes con hiperhidrosis marcada. Puede asociar infección por dermatofitos (Tinea
pedis) |
|
Otitis externa |
Conducto
auditivo externo |
Dolor eritema
y edema del CAE |
En pacientes
diabeticos o inmunodeprimidos puede evolucionar hacia otitis externa maligna con
desarrollo de osteomielitis severa |
|
Ectima gangrenoso |
Región perineal, o cualquier zona del cuerpo |
Lesiones ulceradas, verdosas con escara |
Fiebre, mal estar general, sepsis por gram negativos |
casos
para dx en clase
:casos
per a discussió a classe
casos en word
TEST
Infectious
diseases Society of America: Practice guidelines for the diagnosis and
management of skin and soft tissue infections
www.uv.es/derma Dr. Víctor Alegre de
Miquel


