|
Fases de crecimiento del melanoma |
 |
|
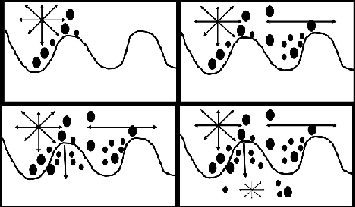
Modelo tradicional: Los melanomas se inician en la epidermis con la proliferación de melanocitos en la unión dermo-epidérmica y de forma gradual presentan un crecimiento intraepidérmico para afectar a toda la epidermis. Cuando inician la fase de crecimiento vertical, rompen la unión dermo-epidérmica y pasan a invadir la dermis papilar, reticular y tejido graso subcutáneo. |
Formas de melanoma: clásicamente se describen 4 formas clínico-patológicas de melanoma cutáneo en relación a la localización anatomica y a su evolución (Tabla III). Las tres formas clínicas: melanoma de extensión superficial, el léntigo melanoma maligno y el melanoma acrolentiginoso, tienen una fase de crecimiento intraepidermica larga, en la cual el tumor está completamente limitado a la epidermis. El cuarto tipo de melanoma, el melanoma nodular, tiene una fase de crecimiento intraepidermica muy corta con el paso al crecimiento vertical (dérmico) rápido. En la actualidad se considera el melanoma como una sola entidad que puede evolucionar hacia una forma clínico-patológica u otra dependiendo de varios factores no bien establecidos como la localización anatómica, y/o el daño solar asociado.
|
Formas clínicas de melanoma maligno | ||||
| Tipo | % | Edad media | Duración de la fase radial | Localización |
| Extensión superficial (SSMM) | 70% | 44 | 1-7 años | Cualquier localización, especialmente en el torso de varones y en las piernas de mujeres |
| Nodular | 10-15% | 53 | meses-2 años | Cualquier localización |
| Lentigo melanoma maligno | 5% | 65 | 5-20 años | Áreas expuestas especialmente en la región malar y pretemporal |
| Acral | 2-8% | 65 | 1-3 años | Palmas, plantas, lecho ungueal, superficies mucosas |
-
Melanoma de extensión superficial: El melanoma de extensión superficial es la forma más frecuente de melanoma ya que representa el 70% de los casos de melanoma. Puede localizarse en cualquier zona del cuerpo, siendo más frecuente en el torso de los varones y en las extremidades inferiores de las mujeres. La edad media en el momento del diagnóstico es de 44 años, y generalmente la lesión tiene una evolución de entre 1 y 5 años. La lesión clínica suele ser una placa pigmentada, palpable, de 1 a 2,5 cm de diámetro, de color marrón oscura, negra o parduzca, que puede presentar áreas claras que reflejan regresión tumoral.
-
Melanoma nodular: El melanoma nodular es la segunda forma de melanoma en frecuencia, representando un 10-15% de los casos de melanoma. Puede desarrollarse en cualquier localización, siendo discretamente más frecuente en torso de los varones y en las piernas de las mujeres. El melanoma nodular tiene una fase de crecimiento corto, entre 6 y 18 meses. Clínicamente la lesión suele tener entre 1 y 2 cm de diámetro y aparece como una lesión papulo-nodular, pigmentada, de coloración marrón oscura, negra con áreas sonrosadas.
-
Lentigo Melanoma: El lentigo melanoma consiste en una lesión pigmentada que se observa en áreas expuestas (con daño solar intenso), especialmente en cara y el cuello de personas mayores. Esta lesión fue descrita en 1890 por Hutchinson y posteriormente por Dubreuilh. En la actualidad se habla de lentigo maligno cuando la lesión está limitada a la epidermis y de lentigo melanoma maligno cuando la lesión se hace invasiva. La incidencia anual de lentigo maligno se sitúa entre 1 y 1,5 por cada 100.000 habitantes, con un porcentaje en aumento, que lo sitúa entre el 4 y el 15% de los casos de melanoma.
-
Melanoma lentiginoso acral: El melanoma lentiginoso acral es el menos frecuente, representando un 2-8% de los melanomas, pero es la forma más frecuente de melanoma en personas de raza negra y asiáticos. Esta forma de melanoma se localiza especialmente en palmas, plantas, y región periungueal. Generalmente se observa en personas mayores, con una edad media de 65 años, y un período de evolución de 2,5 años.
-
Formas menos frecuentes de melanoma
-
Melanoma de mucosas los melanomas en mucosas pueden localizarse a nivel de la mucosa genital, oral o conjuntival. Suelen tener una fase de crecimiento radial o pagetoide semejante a la del melanoma de crecimiento superficial.
-
Melanoma desmoplásico Es una variante clínico-patológica poco frecuente, que se presenta clínicamente como una lesión banal, que posteriormente desarrolla un tumor profundo, fibroso, con predominio de células fusiformes, caracterizado por una tendencia a las recidivas locales múltiples y con gran capacidad de infiltración local mientras que el riesgo desarrollo de metástasis es similar o más bajo que las formas de melanoma.
-
Clasificación molecular del melanoma
A principios de la década de 2010, comenzó a surgir una mejor comprensión de las características moleculares, clínicas y patológicas interrelacionadas de los tumores de melanoma lo que resultó en el desarrollo de un nuevo sistema de clasificación con nueve subtipos o vías de melanoma. Este nuevo sistema fue desarrollado por la OMS y se basa en el sistema clinicopatológico tradicional Cada uno de los subtipos se caracteriza por características epidemiológicas, clínicas, histopatológicas y genómicas distintivas. En relación a los cambios de daño solar y alteraciones moleculares más frecuentemente observadas, se ha propuesto una clasificación molecular del melanoma, pudiendo dividirse los melanomas en 4 grupos:
-
Melanomas sobre piel con daño solar
-
Melanomas con bajo daño solar: incluye los melanomas de extensión superficial con crecimiento pagetoides. Se relacionan con daño solar intermitente y afectan a individuos relativamente jóvenes con un bajo o modeado grado de daño solar en la piel afecta. Histológicamente se caracterizan por una marcada infiltración pagetoide con intensa pigmentación. Esta forma de melanoma se relaciona por un predominio de mutación BRAF p.V600.
-
Melanoma con alto daño solar crónico: corresponde fundamentalmente al lentigo maligno melanoma. Las mutaciones predominantes con en NF1, NRAS y C- KIT
-
-
Melanomas en piel sin daño solar
-
Melanoma acral: Los melanomas acrales se caracterizan por un crecimiento intraepidermico lentiginoso sin estar relacionadas con daño solar. . Estas lesiones se relacionan con mutaciones en multiples puntos en genes como CCND1, KIT y TERT
-
Melanoma de mucosas: estas lesiones no tiene relación con el daño solar. Se han relacionado con mutaciones en KIT y RAS.
-
Dentro de estos subtipos, las lesiones precursoras y las formas intermedias de progresión neoplásica (denominadas colectivamente melanocitomas) fueron reconocidas formalmente por primera vez por la OMS. A diferencia de los nevos, los melanocitomas se caracterizan por tener una segunda mutación genética y un riesgo aumentado, aunque todavía bajo, de progresión a melanoma.
Melanocitomas
Algunos tumores que se clasificaron como nevos o tumores melanocíticos con un
bajo o incierto potencial de malignidad se sabe en la actualidad que albergan
múltiples mutaciones patogénicas. Además de mutaciones que activan la vía MAPK
-que es una vía de señalización alterada en los nevus-, presentan otras
mutaciones involucradas en otros procesos biológicos que producen cambios
fenotipicos. Debido a que presentan múltiples mutaciones conductoras, se
clasifican como melanocitomas de bajo o alto grado según la última clasificación
de la OMS. Muchos melanocitomas se originan en un nevus preexistente, debido a
la adquisición de mutaciones patogénicas secundarias en un solo melanocito, lo
que da lugar a un crecimiento subclonal y a hallazgos histopatológicos
distintivos. En los melanocitomas se incluyen los melanocitomas pigmentados
epitelioides, el melanocitoma penetrante profundo (melanocitomas con activación
de beta-catenina), melanocitomas con inactivación BAP1, los tumores de Spitz
atípicos y los nódulos proliferativos en los nevus congénitos.
Diagnóstico de melanoma:
El diagnóstico clínico de melanoma se basa en el reconocimiento de las características clínicas de las formas de melanoma, es decir la observación de una lesión inicialmente macular pigmentada, de crecimiento asimétrico, de bordes imprecisos y coloración abigarrada con áreas negras y áreas menos pigmentadas y azuladas que representan áreas de regresión. La utilización sistemática de los criterios clínicos resumidos en el acrónimo ABCD (A: Asimetría; B: bordes irregulares; C: coloración heterogénea; D: diámetro mayor de 6mm), es útil para discriminar entre las lesiones benignas y aquellas en las que existe un grado de sospecha. Cuando existen nevus previos la observación de cambios en los mismos también ha de alertar sobre la existencia de melanoma. Los cambios más iniciales son la presencia de cambios en su coloración, prurito, aumento de tamaño y desarrollo de satélites. En lesiones más evolucionadas pueden observarse la aparición de hemorragia y/o ulceración. Además del examen clínico, la realización de fotografías estandarizadas de toda la superficie corporal y la realización de dermatoscopia bien mediante dispositivos de aumento o mediante el análisis digital computerizado de las lesiones pigmentadas, han aumentado la sensibilidad en el diagnóstico de las lesiones sospechosas de melanoma, siendo en la actualidad una ayuda diagnóstica esencial. Cuando existe la sospecha clínica de que una lesión cutánea puede ser un melanoma, la técnica de diagnóstico recomendada es la realización del estudio histológico mediante la práctica de una extirpación-biopsia incluyendo toda la lesión, con un estrecho margen de piel sana.
Histopatologia del melanoma
El estudio histológico del melanoma se basa en la presencia de una proliferación tumoral melanocitica atípica acompañada de cambios epidérmicos y respuesta inflamatoria y dérmica. En las fases iniciales la proliferación de melanocitos atípicos esta limitada a la epidermis (in situ), con presencia de melanocitos en todos los niveles epidérmicos (Crecimiento radial). Los melanocitos atípicos se disponen individualmente y en nidos de tamaño y forma heterogénea. A medida que la lesión progresa puede existir afectación de dermis observándose células tumorales sueltas y en nódulos (Crecimiento vertical) de tamaño y forma variable. Las células del melanoma son de morfología variable, cuboidales o fusiformes y suelen mostrar ausencia de maduración nuclear (reducción del tamaño nuclear en profundidad) así como mitosis y necrosis celular. Los melanomas se acompañan de una respuesta inflamatoria con presencia de infiltrado inflamatorio de predominio linfo-histiocitario que puede ser variable en su distribución e intensidad. Otro hallazgo histológico característico del melanoma es la observación de fenómenos de regresión histológica que consiste en la presencia de un denso infiltrado inflamatorio con presencia de melanófagos y áreas variables de fibrosis dérmica. Existen datos histológicos que son importantes de cara a conocer el pronóstico de un melanoma entre los que se incluyen el grosor en milímetros del tumor (índice de Breslow), la presencia de ulceración, el número de mitosis y la presencia de satelitosis e invasión vascular.
Estadiaje del melanoma
Como hemos mencionado anteriormente el melanoma tiene un comportamiento biológico característico con un crecimiento intraepidermico (crecimiento radial) y un crecimiento dérmico (Crecimiento vertical). En la fase de crecimiento dérmico el melanoma tiene capacidad de producir metástasis. El desarrollo de metástasis es resultado de una serie de eventos que incluyen la existencia de células separadas del tumor primario, la invasión de la membrana basal, la migración hacia el torrente sanguíneo o a la circulación linfática por donde pueden llegar a producir la invasión y crecimiento en otros órgano. Dependiendo en que fase de crecimiento o invasión esté, cambia de forma significativa el pronóstico así como si la enfermedad es local o presenta ya afectación linfática o visceral. Es por ello necesario una vez se diagnostica un melanoma proceder a su estadiaje con fines pronósticos y terapéuticos.
La American Join Cancer Comision, utiliza un sistema de estadiaje de los enfermos con melanoma basado en el estudio del TNM (Tabla IV), que mediante la utilización de datos clínicos y histológicos en relación a las características del tumor (espesor y presencia o no de ulceración), presencia y número de ganglios linfáticos afectos y las características de estos (micrometástasis o macrometástasis) y la presencia o no de metástasis a distancia, permite clasificar a los melanomas en los estadios clínicos dividiendo a los pacientes en los que tienen la enfermedad localizada (estadios I y II) con enfermedad ganglionar y regional (estadio III) y con metástasis a distancia (estadio IV) este sistema de estadiaje permite clasificar a los pacientes en subgrupos homogéneos facilitando su inclusión en ensayos clínicos y la comparación de resultados así como facilita la información pronóstica.
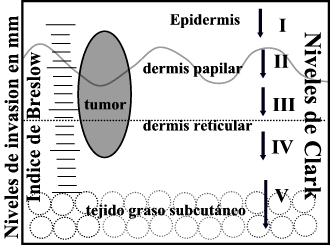
En el estadiaje microscópico del tumor existen dos hallazgos que tienen una gran importancia pronóstica y que son el grosor tumoral, el índice mitótico y la presencia de ulceración. La ulceración es la ausencia histológica de epidermis por encima del tumor. El grosor tumoral se establece utilizando dos sistemas, un sistema basado en la medición milimétrica del grosor (índice de Breslow) y un sistema basado en el nivel cutáneo de invasión (niveles de Clark) (Fig 2). La clasificación de Clark se utiliza con fines orientativos pero no está incluida en la actualidad en el protocolo patológico de diagnóstico de melanoma.
|
Estadiaje clínico del melanoma |
Figura 2 |
|
|
|
| El estadiaje microscópico establece el grosor del melanoma por medio de dos sistemas de medición. Un sistema milimétrico (Índice de Breslow) que establece el grosor tumoral en milímetros por medio de la utilización de una escala milimétrica adaptada al ocular de microscopio y un sistema basado en el nivel cutáneo de invasión |
La medición del espesor tumoral en milímetros, que se conoce como Índice de Breslow, es una variable independiente de otros factores, que determina el pronóstico y la supervivencia de los enfermos con melanoma. Los niveles de invasión o niveles de Clark, describen la invasión de la tumoración en los diferentes niveles cutáneos. El nivel I describe los tumores puramente epidérmicos; el nivel II indica que la tumoración atraviesa la unión dermo-epidérmica con invasión de la dermis papilar; el nivel III describe las tumoraciones que ocupan toda la dermis papilar expandiéndola; el nivel IV indica que la tumoración infiltra la dermis reticular y el nivel V indica la invasión del tejido graso subcutáneo. El pronóstico empeora al aumentar el nivel, pero tiene menos valor que el espesor medido por medio del índice de Breslow y menos valor que el índice mitótico reflejado por el número de mitosis por milímetro cuadrado.
El índice mitótico es un factor pronóstico independiente, el segundo en importancia tras el espesor. La presencia de ulceración en el tumor primario es un factor pronóstico independiente. Los pacientes que presentan ulceración en el tumor primario muestran una supervivencia significativamente menor que los pacientes con un melanoma de identicas características pero no ulcerado.
Otros factores pronóstico: los datos previamente mencionados son los factores pronóstico más importantes, existen otros factores que pueden influenciar el pronóstico como son la localización (los localizados en cuero cabelludo, manos y pies tienen peor pronóstico), el genero (las mujeres suelen presentar mejor pronóstico), la edad (a mayor edad peor pronóstico), la respuesta inflamatoria al tumor (una intensa reacción inflamatoria indicaría un mejor pronóstico), la regresión (indicaría un peor pronóstico) y la invasión vascular (indicaría un peor pronóstico). Se están investigado la utilidad de marcadores que tengan utilidad pronostica en el estudio de enfermos con melanoma como la detección de enzimas de tirosinasa en ganglios linfáticos o sangre para detectar la presencia de tumor en los ganglios o de enfermedad diseminada.
Diagnostico Diferencial
Varias lesiones melanocíticas y no melanocíticas pueden simular un melanoma tanto clínica como histológicamente. Las lesiones que pueden simular melanomas pueden ser: melanociticas (nevus azul, léntigo simple, nevus de vulva), epidérmicas (queratosis seborreica, carcinoma basocelular pigmentado) y vasculares (granuloma piogénico, hemangiomas).
Tratamiento
El diagnóstico precoz es esencial para la curación del melanoma. La extirpación del melanoma cuando éste está limitado a la epidermis y no sobrepasa la membrana basal supone una supervivencia del 100%. Cuando el melanoma rompe la membrana basal e inicia su fase de crecimiento vertical el pronóstico empeora y debe realizarse un tratamiento del tumor primitivo, de la afectación ganglionar y de las metástasis si existen. El pronostico del melanoma en las fases más precoces es excelente a diferencia de los pacientes con melanoma metastásico .
Las pautas de la NCCN definen el estándar de atención para el manejo del melanoma. Todos los casos de melanoma requieren una escisión local amplia. Antes de esta cirugía, se debe tomar una decisión sobre si realizar o no una biopsia de ganglio linfático centinela. La gestión del melanoma que se encuentra más allá de la etapa T1a debe discutirse en un grupo multidisciplinario con oncología quirúrgica y / o médica. En la última década, los inhibidores molécula-cinasa (p. ej., vemurafenib, trametinib) y las inmunoterapias (p. ej., ipilimumab, pembrolizumab, nivolumab) han revolucionado el tratamiento del melanoma metastásico.
El tratamiento del melanoma primario consiste en la extirpación quirúrgica amplia hasta la fascia muscular, con un margen de 1-2 mm de piel normal. Una vez se han realizado esta extirpación se puede realizar el estadiaje microscópico de la lesión y según el nivel de invasión (Espesor de Breslow), el tamaño del tumor y la localización se ha de proceder a una ampliación de la extirpación de entre 1 y 2 cm de margen (Tabla VI). el objetivo de esta ampliación es reducir la posibilidad de recidiva tumoral y de enfermedad residual.
|
Tabla VI
Márgenes quirúrgicos para la extirpación del melanoma primario en relación al espesor tumoral | |
| Espesor tumoral | Margen de extirpación en cm |
| In situ | 5 mm, para conseguir la extirpación completa |
| ≤1 mm | 1 cm |
| 1-2 mm | 1-2 cm |
| 2-4 mm | 2 cm |
| >4 mm | 2-3cm |
Afectación ganglionar
La presencia o no de metástasis linfáticas regionales en los pacientes con melanoma tiene un valor pronóstico en relación a la supervivencia. Si existen metástasis linfáticas, la supervivencia a los 5 años se reduce a un 30-50%. El riesgo de desarrollar metástasis linfáticas está en relación con el espesor del tumor primario. Los tumores in situ no presentan riesgo, los tumores delgados (≤ 1 mm) tienen un riesgo bajo (<5%) y los tumores de espesor medio (>1-≤4 mm) tienen un riesgo de entre un 20-25% de tener metástasis. En los pacientes en los que clínicamente se detecte la presencia de afectación ganglionar puede realizarse la extirpación ganglionar realizándose una disección ganglionar terapéutica. En los pacientes con riesgo de desarrollar metástasis linfáticas pero sin evidencias clínicas de afectación ganglionar puede realizarse un vaciamiento ganglionar de la cadena linfática regional con el objetivo de extirpar las metástasis ganglionares presentes pero clínicamente ocultas, lo que se conoce como disección linfática electiva. La utilidad de la disección linfática electiva ha sido objeto de muchos debates. Los trabajos que defienden la disección electiva sugieren que la extirpación frenaría el proceso metastásico, mientras que los que se oponen sugieren que su extirpación alteraría la respuesta inmune frente al melanoma. Los estudios prospectivos amplios en pacientes con disección electiva o sin ella no demuestran diferencias en la supervivencia a largo plazo, por lo que es una técnica que en la actualidad está prácticamente abandonada. (calculadora del riesgo de positividad del ganglio centinela).
Para poder diferenciar entre los pacientes con afectación ganglionar clínicamente oculta y los pacientes sin metástasis linfática, se ha desarrollado una técnica que se conoce como el estudio del ganglio centinela, (Video Dr. Morton NEJM., video Nejm 2011). Esta técnica se basa en el concepto de que la progresión del cáncer se realizaría de una forma ordenada y que en un primer estadio las metástasis se localizarían en los ganglios linfáticos. El primer ganglio al cual las células neoplásicas metastatizan se denomina ganglio linfático centinela. Por medio de la utilización de colorantes o de isótopos inyectados en la zona del tumor original, se puede localizar dicho ganglio y estudiarlo histológicamente, lo que permite identificar a aquellos pacientes en los que existe metástasis linfáticas clínicamente ocultas. El valor de la realización del estudio de ganglio centinela en el estadiaje del melanoma está bien establecido aunque su impacto en la supervivencia está menos definida. El estatus del ganglio centinela (positivo o negativo) es considerado como el factor más importante para valorar la recurrencia y la supervivencia en pacientes con melanoma. Las recomendaciones para la realización del estudio del ganglio centinela están resumidas en la tabla. La realización del estudio de ganglio centinela debe ser discutido y ofrecido con los pacientes con melanoma de >1 mm de espesor y en situaciones determinadas. El estadiaje de los ganglios linfáticos regionales identifica a los pacientes con melanoma y metastasis ocultas y clasifica a los pacientes en un estadio III. Un meta-análisis con 25240 pacientes mostro un riesgo de un 5% o menor de recurrencia nodal regional tras un ganglio centinela negativo. El tratamiento quirúrgico de los pacientes con metastasis locoregionales está en constante evolución. Si bien la realización de una diseccion de la caden aganglional completa ha sido el estandart del tratamiento de pacientes con biopsia de ganglio centinela positivo, , esta es una técnica que en la actualidad se está abandonando. LOs estudios clinicos sugieren que el seguimiento de estos pacientes y la instauración de tratamiento adyuvante es la terapia más indicada en este grupo de pacientes.
Tratamiento coadyuvante y tratamiento de la enfermedad metastásica
El tratamiento de los pacientes con metástasis linfática consiste en la extirpación del tumor primario y en la disección ganglionar terapéutica. Tras la realización del tratamiento quirúrgico, estos pacientes precisan tratamiento coadyuvante para aumentar el período libre de enfermedad. Hasta antes del año 2010, se habían utilizado muchos tipos de tratamientos: quimioterapia, inmunoterapia inespecífica (tratamiento con el Bacilo de Calmette-Guerin, levamisol), inmunoterapia activa específica, inmunoquimioterápia, perfusión quimioterápica aislada en un miembro para melanomas de extremidades y radioterapia. Sin embargo, ninguna de estas modalidades terapéuticas habia mejorado la supervivencia de los pacientes afectos.
Dado que el melanoma metastásico es, por lo general, incurable, la finalidad de los tratamientos es paliativa. Las técnicas utilizadas incluyen la quimioterapia, la radioterapia y la cirugía. La quimioterapia más utilizada consiste en la administración de un solo agente quimioterápico -la dacarbazina- que consigue unas respuestas parciales en el 15-25% de los pacientes, pero que generalmente suelen ser de corta duración.
La utilización de poliquimioterápia no mejora los porcentajes de remisión y supervivencia. La perfusión aislada de un miembro con melfalan e hipertermia, mejora los casos de enfermedad localizada en una extremidad, pero no mejora la supervivencia de esos enfermos y puede asociar complicaciones graves. La aplicación de radioterapia está indicada en el tratamiento local de recidivas tumorales y de las metástasis, especialmente de las localizadas en el sistema nervioso central. En algunos pacientes con enfermedad metastásica localizada, la extirpación quirúrgica de las metástasis puede prolongar su supervivencia.
Modificadores de la respuesta biológica al melanoma: El melanoma metastático es un tumor con mala respuesta a la quimioterapia, pero es además un tumor inmunogénico, en el cual es posible observar remisiones espontáneas y existen muchos indicios de respuestas inmunes anti-tumor. Estos datos hacen sugerente que la inmunoterapia pueda tener un papel en el tratamiento de los casos de melanoma metastático. En pacientes con metástasis linfática regional se administra inmunoterapia con interferón que a dosis altas ha demostrado beneficio en los períodos libres de enfermedad pero no en la supervivencia, siendo mal tolerado, existiendo varios protocolos de estudio de la respuesta a dosis más bajas.
Nuevas dianas terapéuticas: El tratamiento de la enfermedad metastásica diseminada es casi siempre incurable con una supervivencia media de 6-9 meses, una supervivencia al año del 25% y a los 3 años del 15%, siendo hasta hace poco la dacarbacina la única medicación aprobada. Esta situación ha cambiado de forma radical ya que se ha demostrado una supervivencia mucho mayor con la utilización de dos aproximaciones terapéuticas, la inmunomodulación y la utilización de medicaciones contra las mutaciones diana en las células tumorales.
-
Inmunomodulación:
-
La utilización del propio sistema inmune en el tratamiento del melanoma fue siempre un objetivo que se fundamentaba en la frecuente observación de fenómenos inmunes asociados al melanoma. El melanoma es uno de los tumores más inmunogénicos en el que se observan fenómenos de regresion y presencia de infiltración de linfocitos T infiltrando el tumor y las metástasis (TILs). Inicialmente se utilizó el interferon-α. Mas recientemente se han desarrollado nuevas molécula dirigidas contra dianas inmunes con una respuesta terapéutica superior y un aumento de la supervivencia y del período libre de enfermedad.
-
Anticuerpo anti CTLA-4: El receptor es un receptor proteico situado en la membrana celular de los línfocitos T. La unión del CTLA-4 a las células de presentación antigénica produce una inhibición de las células T. El bloqueo de esta inhibición con una molécula anti CTLA-4 (ipilimumab) aumenta la proliferación y activación de los linfocitos T. La utilización del Ipilimumab ha demostrado un beneficio estadisticamente significativo en la supervivencia global en enfermos con melanoma estadio III y IV. La administración de ipilimumab está asociada a diversos efectos secundarios, relacionados con el sistema inmune, que incluyen manifestaciones digestivas (diarera, colitis) endocrinas (hipofisitis, hipo e hipertiroidismo ye insuficiencia suprarrenal). , se ve inhibida por la estimulación del receptor CTLA-4
-
Anticuerpo anti PD1: El receptor de muerte programada-1 (PD-1) se expresa en la superficie de las células T CD8 + específicas de antígeno. La unión del receptor PD1 a su ligando PD-L1 en los tejidos normales, se previene una respuesta inmune exagerada y se mantiene una tolerancia a los autoantígenos. La expresión de PD-L1 en las células de melanoma inhube la activación y proliferación de células T. Los anticuerpos anti PD1 bloquean el recceptro PD1 en las células T previniendo su unión con el PD-L1 y la inhibición de las células T consiguiente. Los antagonistas del receptor PD-1, nivolumab y pembrolizumab bloquean el eje PD-1 / PD-L1(figura). Los resultados de ensayos clínicos recientes que utilizan antagonistas de PD-1 han mostrado altas tasas de respuesta clínica. Los ensayos clínicos iniciales para pembrolizumab mostraron un impresionante 38% tasa de respuesta, con una supervivencia media superior a 7 meses. Los resultados de un número creciente de ensayos clínicos están estableciendo rápidamente los antagonistas de PD-1 como la estrategia de tratamiento de melanoma más efectiva disponible en la actualidad.
-
Vacunas: El papel de las vacunas en el tratamiento del cáncer es la estimulación de una respuesta inmune sistémica del huésped contra las células cancerosas. La vacuna más prometedora para el melanoma es una vacuna oncolítica derivada de un virus de herpes simple modificado conocido como T-VEC. Los virus oncolíticos infectan y destruyen preferentemente las células cancerosas. Esto ocurre no solo induciendo respuestas inmunitarias contra las células cancerosas, sino también interrumpiendo directamente los procesos metabólicos. los beneficios de supervivencia siguen siendo bajos y se limitan en gran medida a los pacientes con melanoma en estadio III.
-
-
Medicaciones dirigidas a las mutaciones presentes en el melanoma. Inhibidores BRAF y MEK: las mutaciones en BRAF están presentes en aproximadamente el 50% de melanomas, especialmente aquellos relacionados con la exposición intermitente al sol. BRAF juega un papel importante en la proliferación celular por medio de la activación de la via protein cinasa activada por mitogeno (MAPK:mitogen-activated protein kinase). Los inhibidores BRAF (Vemurafenib y Dabrafenib) son capaces de inducir respuestas muy importantes en melanomas estadio III y IV irresecables. La mayoría de pacientestratados desarrollan una resistencia a los inhibidores, que se explica por una reactivación de BRAF o por mutaciones en MEK. La utilización combinada de inhibidores MEK (Trametinib, Cobimetinib) produce una respuesta terapéutica superior con mejores datos en supervivencia global y periodos libres de enfermedad. La utilización combinada esta sujeta a diversos efectos secundarios dermatologicos, con fotosensibilidad y el desarrollo de neoplasias cutáneas (especialmente con inhibidores BRAF).
Prevención y control del melanoma
La diferencia pronostica entre los melanomas delgados (Nivel I, y II) y los gruesos (III, IV y V), hace que en esta enfermedad la prevención y el diagnóstico precoz sean sumamente importantes. La prevención debe incluir medidas para preservar la capa de ozono, regular la utilización y publicidad de cabinas de UVA con fines cosméticos e insistir en la educación publica sobre protección solar y uso de filtros solares especialmente en niños y adolescentes. La utilización de filtros solares parece prevenir el desarrollo de cáncer cutáneo no melanoma, sin embargo diversos estudios han relacionado el uso de filtros solares de bajo índice de protección (menor de 10) con un riesgo mayor de desarrollo de melanoma, relacionándose con una mayor tolerancia de los pacientes a la radiación con un aumento de las horas de exposición. Los profesionales sanitarios y, especialmente, los médicos generales, deben tener el hábito de diagnóstico del melanoma y sus lesiones precursoras durante un examen físico rutinario. Una vez se diagnostica a un enfermo de melanoma, este debe seguir controles médicos periódicos con los objetivos principales de detectar precozmente una recidiva de la enfermedad y detectar un posible segundo melanoma. La recidiva de la enfermedad puede presentarse en forma localizada o en tránsito (25% de casos), en forma de enfermedad regional (26-60% de casos) o a distancia (15-20% de casos). Los métodos más eficaces para detectar la enfermedad recurrente son la realización de la historia clínica y el examen físico, estando en estudio el valor que puede tener la realización de ecografía linfática. Asimismo, debe enseñarse a los enfermos a realizarse controles ya que en un porcentaje elevado son ellos mismos los que van a detectar la presencia de recidiva de la enfermedad.
www.uv.es/derma Dr. Víctor Alegre de Miquel