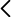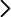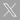A pesar de los enormes esfuerzos para combatir el cáncer, su incidencia se incrementará a 22 millones de nuevos casos anuales para el año 2030. Para abordar este problema tenemos que reconsiderar el diagnóstico y desarrollar estrategias terapéuticas más eficaces.
Las células somáticas, invariablemente, experimentan un cese irreversible de la proliferación y una funcionalidad alterada después de un número finito de divisiones. Este proceso fisiológico se denomina senescencia celular. Las células senescentes se acumulan en los tejidos, acelerando así el envejecimiento y contribuyendo al desarrollo de la enfermedad.1 Por otra parte, varias evidencias recientes apoyan el concepto de que la acumulación de células senescentes puede conducir al desarrollo de cáncer, y de que su eliminación puede ser terapéutica.2-5 Por lo tanto, las estrategias para eliminar o detectar células senescentes son de un interés fundamental. En particular, el diseño de tales terapias contribuiría a la prevención del cáncer (por eliminación de las células senescentes precancerosas) y puede impulsar la idea a largo plazo que el rejuvenecimiento humano podría ser posible. Hay pruebas recientes de que la eliminación de células senescentes rejuvenece tejidos in vivo y aumenta la longevidad. Por ejemplo, se ha demostrado que inhibidores de la familia de Bcl2 (navitoclax) inducen preferentemente la muerte de células senescentes y rejuvenecen animales con progerias.6-8
Por otra parte, el diseño de sistemas capaces de detectar una población de células senescentes anormal, podría ser utilizado como herramienta para identificar las personas que pueden desarrollar un cáncer en el futuro. Un abordaje para lograr el objetivo de eliminar / detectar células senescentes debe relacionarse con el desarrollo de las dispositivos de transporte capaces de liberar su carga selectivamente en este tipo de células. Desgraciadamente, a día de hoy, no existen tales sistemas de liberación dirigidos.
En este contexto hemos descrito recientemente nanopartículas de sílice mesoporosa (MSN), capaces de liberar su carga de manera selectiva en las células senescentes con una alta especificidad y sin toxicidad asociada. Nuestra estrategia conlleva el uso de MSNs recubiertas con un galactoligosaccharide (GOS) y la presencia específica de la β-galactosidasa asociada a la senescencia (SA-β-gal) en células senescentes. Estas MSN recubiertas de GOS fueron capaces de liberar su carga de manera selectiva en fibroblastos humanos senescentes de pacientes con disqueratosis congénita mientras que no se detectó liberación en experimentos control con células no senescentes.9 Hasta donde sabemos, que esta es la primera vez que se ha descrito una (nano) terapia dirigida para las células senescentes.
Estos y otros resultados preliminares (vide infra) sugieren que por la elección de una carga apropiada, la eliminación (por ejemplo, usando un fármaco citotóxico) y detección (por ejemplo, usando colorantes de señalización) de las células senescentes podría ser posible.
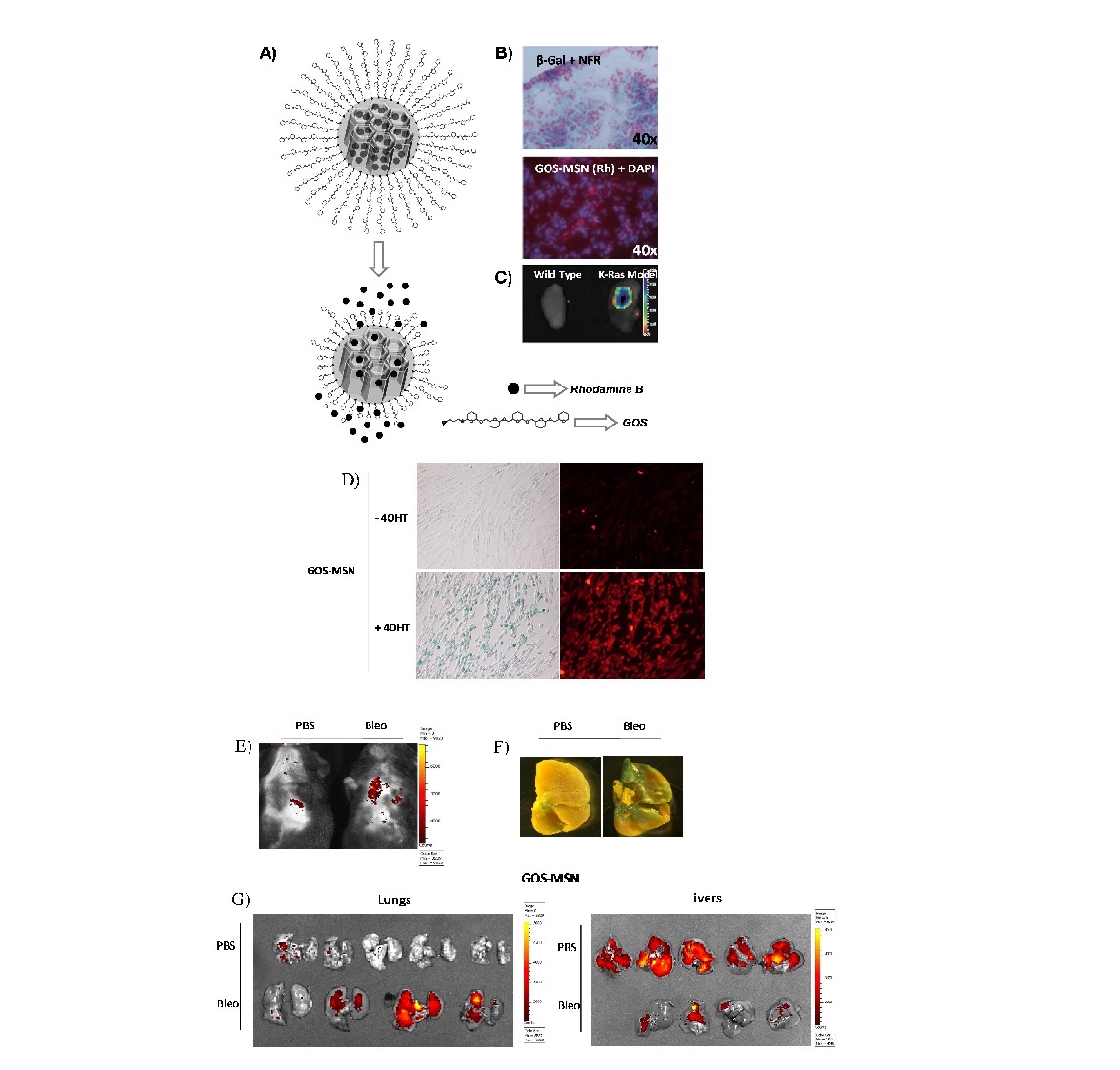
Varias líneas de evidencia nos animan a predecir un resultado positivo en las pruebas de concepto in vivo resultado de nuestro enfoque: i) Los estudios in vitro demostraron que la carga se mantuvo en las nanopartículas GOS-MSN (liberación cero) en ausencia de β-gal, mientras que en presencia de β-gal, se observó la liberación de la carga debido a la hidrólisis del GOS por la β-gal ii). El nanomaterial GOS-MSN liberó selectivamente su carga en células de levadura que sobreexpresan β-gal. iii) El nanomaterial GOS-MSN liberó selectivamente su carga en fibroblastos humanos senescentes DC1787 y en células X-DC1774 y X-DC4646 de pacientes con Disqueratosis Congénita. No se observó liberación en células no senescentes tales como células H460 de cáncer no microcítico de pulmón. iv) Criosecciones pulmonares derivados de un modelo animal de carcinoma de pulmón inducido por el oncogén K-Ras se enriquecen en células positivas para β-gal. Incubamos estas criosecciones con el nanomaterial GOS-MSN cargada con rodamina y las analizamos por microscopía de fluorescencia. La fluorescencia de rodamina se detectó específicamente en las zonas tumorales de las criosecciones. v) Por último, la incubación de los pulmones aislados con carcinomas con el nanomaterial GOS-MSN cargado con rodamina reveló que la fluorescencia de Rodamina se localizaba exclusivamente en las zonas tumorales. No se detectó tinción en los pulmones normales aislados.
Por otro lado, estudios basados en células utilizando GOS-MSN cargadas con doxorrubicina han demostrado que las nanopartículas se internalizan en el retículo endoplasmático (ER). En el caso de las células senescentes, la doxorrubicina se libera de manera eficiente en el ER y las células mueren en aproximadamente 7 horas. Por el contrario, en células normales no senescentes, las nanopartículas también entran en la ER pero liberan la doxorrubicina muy lentamente y de manera ineficiente, resultando en una muerte celular sólo parcial después de más de 12 horas.
También hemos realizado estudios in vivo utilizado dos modelos murinos de senescencia, en particular modelos murinos de fibrosis pulmonar inducida por bleomicina y senescencia inducida por palbociclib en xenoinjertos tumorales. En ambos casos, se ha observado que el nanomaterial GOS-MSN que transportan rodamina o doxorrubicina libera su carga preferentemente en los tejidos senescentes. Los datos preliminares muestran una tendencia terapéutica en los ratones tratados con GOS-MSN cargados con doxorrubicina (reducción parcial de la fibrosis y la reducción parcial del tamaño del tumor). En este momento nos encontramos optimizando la dosificación para lograr un efecto terapéutico completo. El objetivo de estos estudios es restringir la liberación del agente quimioterapéutico (doxorrubicina, u otros) en las lesiones senescentes, lo que reduciría sustancialmente los efectos tóxicos de la quimioterapia.
A partir de estas pruebas previas, el presente proyecto se centra en validar en modelos murinos GOS-MSN (o nanodispositivos similares) con liberacion "cero", pero con capacidad de liberar su carga de manera selectiva en las células senescentes. Al final de este proyecto, se espera disponer de una Plataforma Tecnológica en Oncología que podría convertirse en la primera terapia de su clase, listo para entrar en la fase de validación preclínica. Creemos que este enfoque podría abrir nuevas vías para el desarrollo de aplicaciones terapéuticas innovadoras para prevenir / tratar el cáncer (a través de la eliminación selectiva de las células senescentes) o enfermedades relacionadas con el envejecimiento.
RAMON MARTINEZ MAÑEZ
Centro Nacional de Investigaciones Oncológicas (CNIO)
Instituto de Salud Carlos III