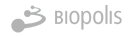Las enfermedades humanas que se originan en reservas no humanas, las zoonosis, constituyen el 75% de las enfermedades infecciosas emergentes y suponen una importante amenaza para la salud pública. En el caso particular del Ébola, la epidemia de 2014 en el África occidental ha sido la mayor registrada hasta ahora, afectando a decenas de miles de personas con tasas de mortalidad cercanas al 75%. Además, el virus del Ébola (EV) diezma la población de grandes simios, lo que supone un peligro para la conservación, representa una importante amenaza en todo el mundo por la importación de infecciones y su posible uso indebido como arma biológica, y tiene consecuencias económicas y humanitarias drásticas.
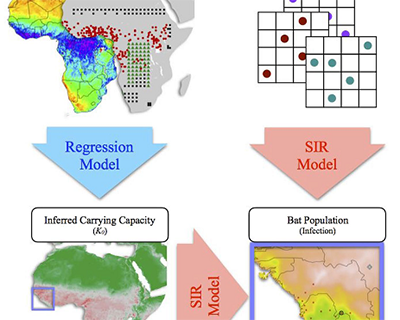
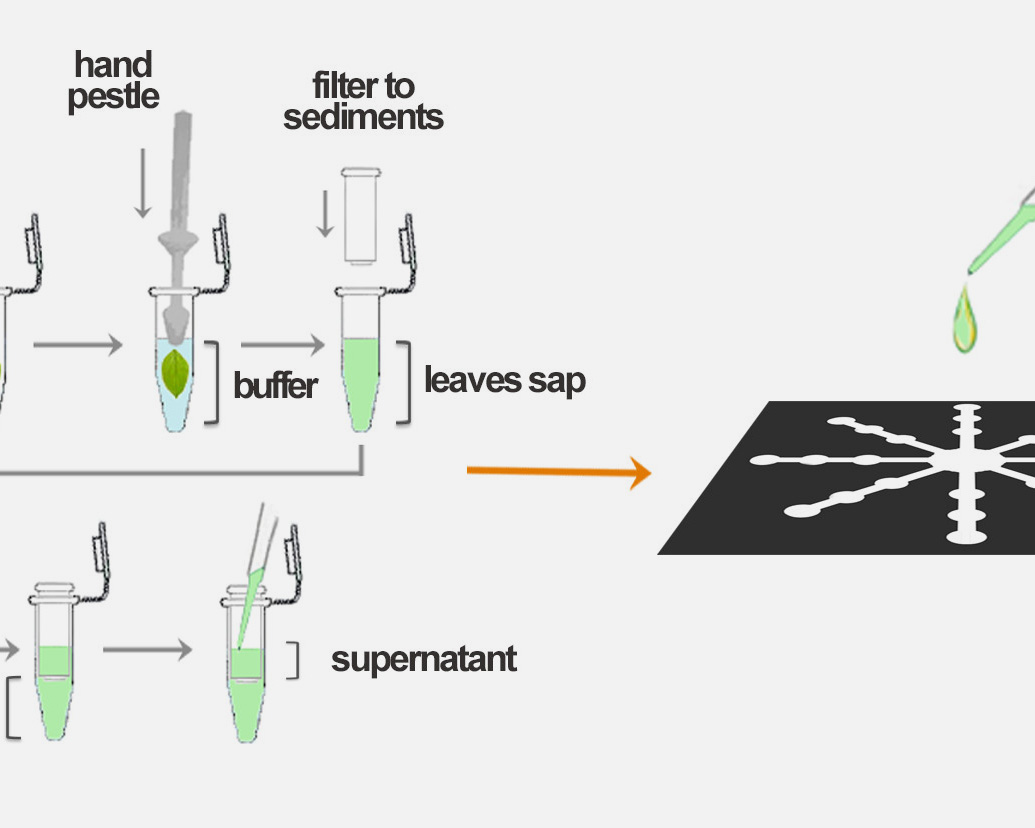
La generación de alteraciones mitóticamente estables en la expresión de los genes debido a marcas epigenéticas es una manera rápida y relativamente duradera de establecer una memoria genómica de los acontecimientos de estrés pasados. La desregulación desencadenada por el medio ambiente de los factores genéticos asociados a las maquinarias epigenéticas también puede dar lugar a una plasticidad fenotípica y a la mitigación del estrés. Por lo tanto, la maquinaria epigenética del huésped puede suponer una presión selectiva importante, pero en gran medida no medida, sobre los patógenos. Los virus de las plantas ofrecen un modelo conveniente para estudiar este tipo de interacciones. En primer lugar, se propone un experimento de evolución a gran escala para comprobar cómo evolucionan e interactúan las poblaciones de virus en plantas con vías epigenéticas comprometidas o mejoradas. Las plantas de Arabidopsis thaliana con mutaciones en genes clave asociados a marcas de cromatina activas o represivas, incluida la metilación del ADN y la modificación de las histonas, se enfrentarán a linajes independientes del virus del mosaico del nabo (TuMV).
La secuenciación masiva en paralelo o de nueva generación (NGS) ha supuesto una revolución en los estudios genéticos, teniendo importantes aplicaciones en investigación y en clínica. Algunas son el estudio del genoma, transcriptoma, microbioma, metiloma, el diagnóstico genético y de medicina personalizada, como farmacogenética y la detección de marcadores tumorales somáticos, estudios de mutaciones tumorales en ADN circulante, determinación de la tasa de mutación para estudios de inmunoterapia para oncología. Una aplicación importante es el estudio de regiones concretas del genoma para muchos de los estudios clínicos o de investigación, principalmente de uno o varios genes (panel de NGS) debido a los elevados costes de estudios de genoma completo.
La resistencia a los antibióticos y la ingeniería de tejidos/medicina regenerativa han sido reconocidas como dos de los grandes retos de investigación de la Biotecnología. Aunque aparentemente inconexos, argumentamos que proporcionar respuestas cuantitativas a estas cuestiones requiere un enfoque común desde el punto de vista de la mecanobiología. Por un lado, la lectura fenotípica característica de la resistencia a los antibióticos (y más en general de la respuesta al estrés en las bacterias) es la filamentación.
La habilidad de resolver estructuras poblacionales en alta resolución y profundidad es esencial para comprender la evolución viral y la patogénesis. En este proyecto implementamos técnicas de secuenciación basadas en una extrema fidelidad hacia la última generación para poder abordar las cuestiones clave de la evolución viral y la patogénesis.
Contrato de asesoramiento y apoyo técnico con Empresa EVERIS.
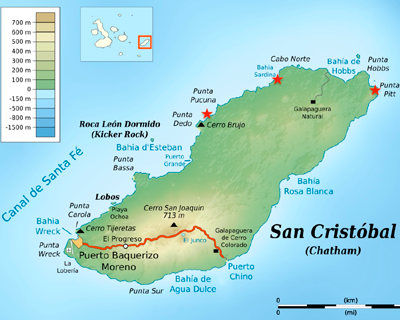
Coordinado por el Instituto de Biología Integrativa de Sistemas (I2SysBio) y la Universidad San Francisco de Quito. El proyecto explora la presencia de microorganismos con potencial generador de electricidad de las comunidades microbianas presentes en los sedimentos de lagunas saladas y salobres de la isla San Cristóbal del archipiélago de las Galápagos. Galápagos explora la producción de electricidad de muestras ambientales, caracteriza el contenido metagenómico de las comunidades microbianas y la correlación de la presencia de especies electrogeneradoras con parámetros ambientales como el pH, salinidad, temperatura y oxígeno disuelto.
Coordinado por el Instituto de Biología Integrativa de Sistemas I2SysBio) y la ICTS Laboratorio Subterráneo de Canfranc. El proyecto estudia el contenido y la variabilidad espacial de las comunidades microbianas presentes en muestras de rocas calizas del Pirineo a cientos de metros de profundidad gracias al acceso por el túnel de Somport, situado en el Pirineo Central y que une los valles del Aragón (España) y de Aspe (Francia). Gollum explora un ambiente extremo poco conocido, caracterizado por pocos nutrientes, diversos sustratos fisicoquímicos, bajos niveles de cualquier tipo de radiación y pequeñas fluctuaciones térmicas. La presencia de ADN nativo y la identificación de un alto contenido de arqueas y su correlación con metales presentes son algunos de los resultados más relevantes del proyecto y abren la posibilidad de múltiples cuestiones, comenzando por resolver si el material genómico identificado corresponde a ADN reliquia o por el contrario a microorganismos vivos aislados del exterior desde decenas de millones de años.


 Evaluación de los riesgos de los brotes de Ébola mediante la modelización probabilística de la dinámica zoonótica de los quirópteros y los factores socioeconómicos
Evaluación de los riesgos de los brotes de Ébola mediante la modelización probabilística de la dinámica zoonótica de los quirópteros y los factores socioeconómicos
 EPICOVIR
EPICOVIR
 EOSAL_CLINIC
EOSAL_CLINIC
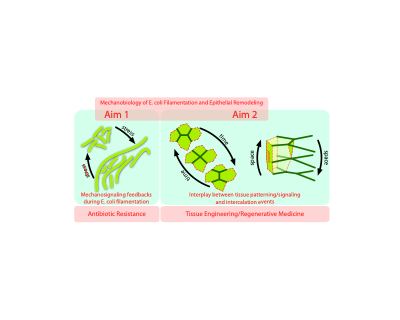 Mecanobiología de la filamentación de E. coli y remodelación epitelial
Mecanobiología de la filamentación de E. coli y remodelación epitelial
 AICO
AICO
 Asesoramiento para la ejecución del proyecto de desarrollo de una aplicación de autoría de listados de secuencias de nucleótidos y aminoácidos en formato ST26
Asesoramiento para la ejecución del proyecto de desarrollo de una aplicación de autoría de listados de secuencias de nucleótidos y aminoácidos en formato ST26
 GALAPAGOS
GALAPAGOS
 GOLLUM
GOLLUM
 PLANT-PREDICTOR
PLANT-PREDICTOR
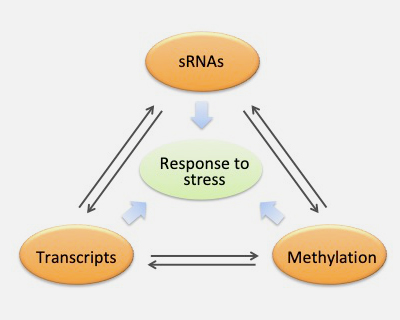 EGReNMel
EGReNMel
 COV-CRISPIS
COV-CRISPIS
 NETFRUIT
NETFRUIT
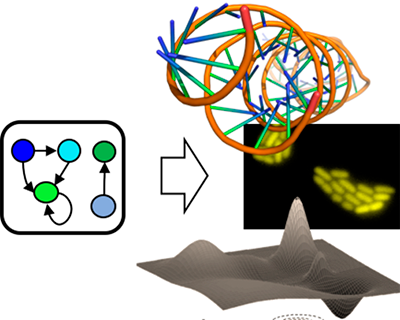 SYSY-RNA
SYSY-RNA
 RNAct
RNAct
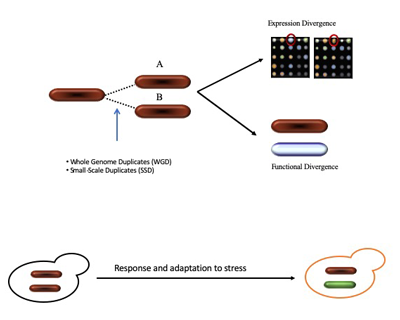 EvolDup2Inno
EvolDup2Inno
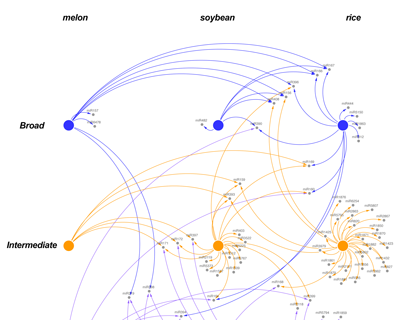 Validación funcional de las redes de sncRNAs que regulan la respuesta a estrés en melón
Validación funcional de las redes de sncRNAs que regulan la respuesta a estrés en melón
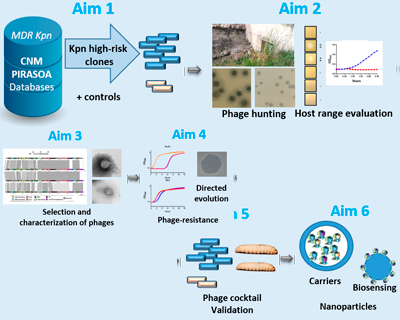 PHAGTHERKpn
PHAGTHERKpn
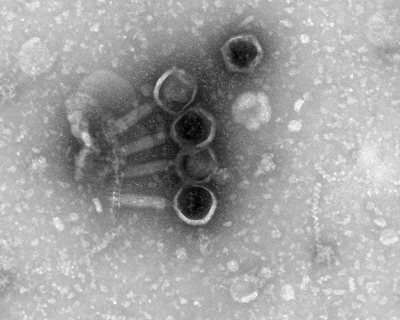 Superfago
Superfago
 PhageMabs
PhageMabs
 PTI+: Transmisión y contención
PTI+: Transmisión y contención
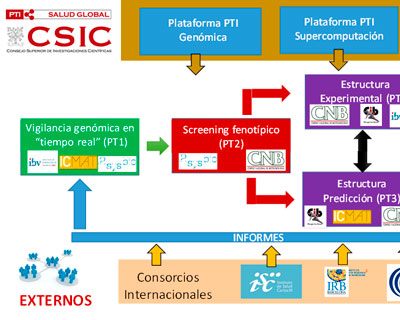 Vigilancia genómica
Vigilancia genómica
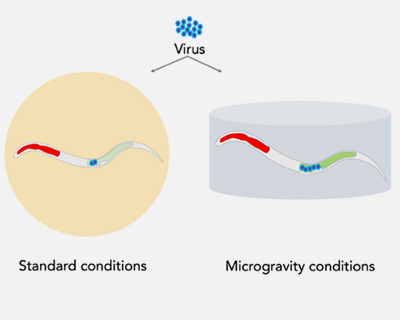 SpaceWorms
SpaceWorms
 Mutaciones
Mutaciones
 Antiviral platform
Antiviral platform
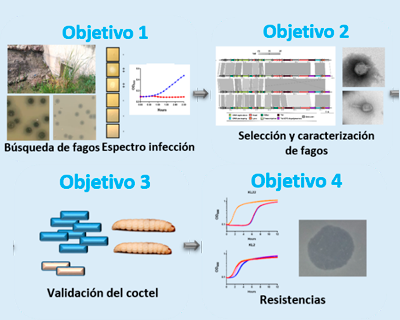 FagoterapiaKpn
FagoterapiaKpn
 FecOrSARS
FecOrSARS
 COVID-19: acción antiinfecciosa y antinflamatoria de las moléculas del parásito inmunomodulador en un formato sintético de uso seguro
COVID-19: acción antiinfecciosa y antinflamatoria de las moléculas del parásito inmunomodulador en un formato sintético de uso seguro
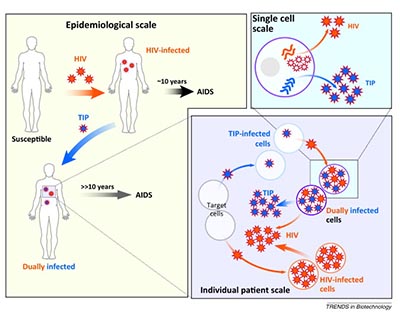 CoV2TIP
CoV2TIP
 CaeVirus
CaeVirus
 EnvironmentalCOVID
EnvironmentalCOVID
 BlockAce
BlockAce
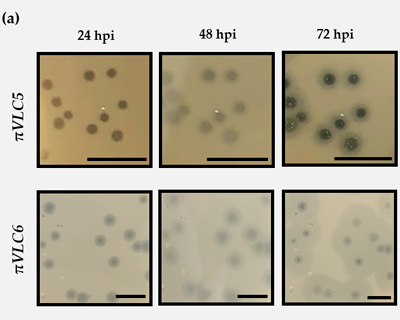 IsolationKpnPhages
IsolationKpnPhages
 SeqCOVID
SeqCOVID
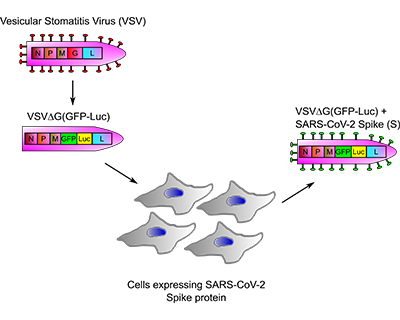 ANTICOR
ANTICOR
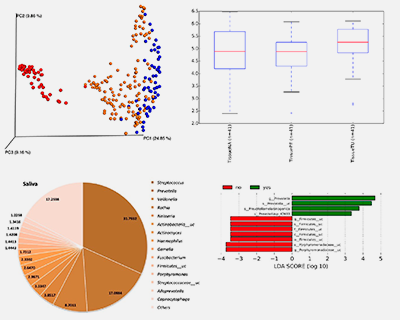 MicroHNSCC
MicroHNSCC
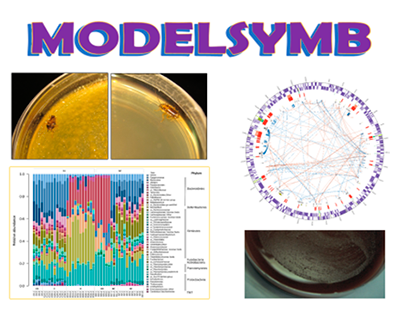 MODELSYMB
MODELSYMB
 FUNGENAPHID
FUNGENAPHID
 eGUT
eGUT
 STOP
STOP
 CINCHRON
CINCHRON
 GECONAMBRO
GECONAMBRO
 GREEN
GREEN
 InGEMICS
InGEMICS
 CONCISE
CONCISE
 MICROLYNCH
MICROLYNCH
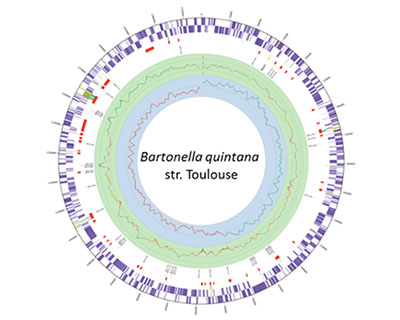 MICROEVO
MICROEVO
 STABIOME
STABIOME
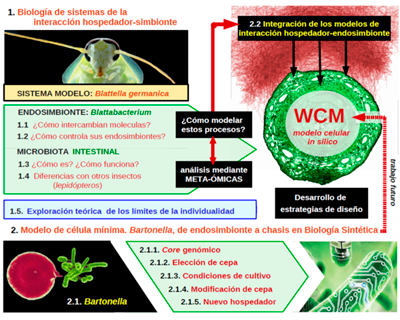 SimbVención
SimbVención
 Grupo 2 CIBEResp
Grupo 2 CIBEResp
 ENTOMOPLAST
ENTOMOPLAST
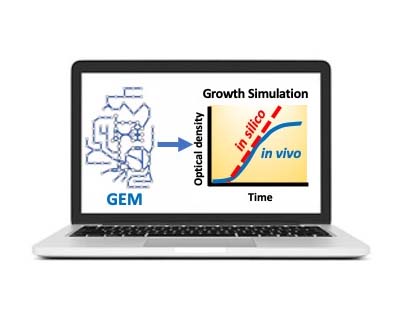 BactGem
BactGem
 MIPLACE
MIPLACE
 SETH
SETH
 IBER-XYFAS
IBER-XYFAS
 PROFERTILITY
PROFERTILITY
 BIOROBOOST
BIOROBOOST
 NutOxWineYeast
NutOxWineYeast
 HELIOS
HELIOS
 MICROBIOSOL
MICROBIOSOL
 SINNBIOSIS
SINNBIOSIS